
【题目】下列五种物质中,①Ar ②CO2 ③SiO2 ④Ba(OH)2 ⑤K2S,含有共价键的物质有________(填序号)。分别写出CO2、Ba(OH)2的电子式________、________。
【答案】②③④ ![]()
![]()
【解析】
共价键为非金属原子之间形成的化学键;二氧化碳中存在两个碳氧双键,使C、O原子最外层都达到最外层8个电子;Ba(OH)2是离子化合物,由Ba2+离子和OH-离子构成。
①Ar为单原子分子,不含化学键;
②在CO2分子中,C和O以共价键相结合;
③在SiO2中,Si和O原子之间以共价键相结合;
④Ba(OH)2是离子化合物,由Ba2+离子和OH-离子通过离子键结合构成,在OH-离子中氢和氧以共价键结合;
⑤K2S为离子化合物,由硫离子和钾离子通过离子键结合成,无共价键;
所以上述物质中含有共价键的物质序号为②③④;
在CO2分子中,C原子与2个O原子通过四对共用电子对结合,使C、O原子最外层都达到最外层8个电子,电子式为:![]() ;
;
Ba(OH)2是离子化合物,由Ba2+离子和OH-离子构成,Ba(OH)2的电子式为:![]() 。
。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
【题目】现有四种有机化合物A.C2H4 B.![]() C.CH2=CH-CH=CH2 D.HOOCCH2CH2CH2Cl
C.CH2=CH-CH=CH2 D.HOOCCH2CH2CH2Cl
(1)C与Br2按物质的量之比1∶1反应后的产物是_________、_____________
(2)B的分子式是_________
(3)下列有关叙述正确的是_________
A.C可能的加聚产物是![]()
B.D中的官能团名称分别是酸基、氯原子
C.B能使酸性KMnO4溶液褪色
D.A生成的聚合物的链节是—CH2-CH2—
(4)D经过三步反应生成五元环酯,
HOOCCH2CH2CH2Cl![]() E
E![]() F
F![]()
![]()
则E的结构简式_________,F生成五元环酯的化学方程式______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)偏铝酸钠溶液中逐滴加入盐酸至过量,可观察到的现象是____________________,反应的离子方程式是____________________________、____________________________。
(2)偏铝酸钠溶液中持续不断地通入二氧化碳,可观察到的现象是________________,反应的离子方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用氯酸钾与密度为1.19gcm﹣3,溶质质量分数为36.5%的浓盐酸反应制取氯气。
I.反应方程式如下:___KClO3+ HCl= KCl+ Cl2↑+ H2O
(1)配平方程式,并用双线桥法表示上述反应中电子转移的方向和数目。
(2)若反应中被氧化的盐酸为5mol,则生成的氯气体积为__________(标准状况下)。
II.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。请回答下列问题:
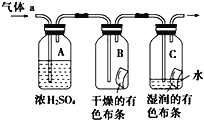
(1)证明氯气和水反应的实验现象为__________,反应的化学方程式是__________。
(2)若将氯气通入石灰乳制取漂白粉,反应的化学方程式是__________,漂白粉溶于水后,遇到空气中的CO2,即产生漂白、杀菌作用,反应的化学方程式是__________。
III.乙同学用上述浓盐酸配置0.100 mol·L-1的稀盐酸480 mL,下列说法正确的是__________。
A.取用240 mL的容量瓶
B.应量取上述浓盐酸的体积为4.2mL
C.定容摇匀后发现液面低于刻度线,再加蒸馏水与刻度线相切,所配溶液浓度偏小
D.定容时,仰视刻度线所配溶液浓度偏大
E.量取上述浓盐酸的体积时俯视刻度线所配溶液浓度偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有氢气放出,下列叙述不正确的是( )
A.NH4H是离子化合物,含有离子键和共价键
B.NH4H与水反应时,NH4H是还原剂
C.NH4H投入少量的水中,有两种气体产生
D.NH4H溶于水,所形成的溶液成酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。它可以按下列方法进行制备:SiO2![]() Si(粗)
Si(粗) ![]() SiHCl3
SiHCl3![]() Si(纯)。下列说法正确的是( )
Si(纯)。下列说法正确的是( )
A.反应①的化学方程式为SiO2+C![]() Si+CO2↑
Si+CO2↑
B.反应①②③中每生成或消耗1 mol Si,转移4 mol电子
C.二氧化硅与氢氟酸反应,而硅不能与氢氟酸反应
D.SiHCl3(沸点31.8 ℃)中含有少量的SiCl4(沸点57.6 ℃),通过蒸馏(或分馏)可提纯SiHCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质:①.Cu ②.NaCl晶体 ③.NaHSO4 ④.CO2 ⑤.CaO ⑥HCl ⑦.稀H2SO4 ⑧. 熔融Ba(OH)2 ⑨.C2H5OH ⑩.NaCl溶液。
属于电解质的是(填序号,下同)_____,属于非电解质的是_____,能导电的是______。
(2)写出下列物质在水溶液中的电离方程式:
①NaHSO4 ___________________________;
②Al2(SO4)3 ________________________________;
③NH4NO3 ________________________。
(3)按要求写出下列方程式:
①写出硫酸铜溶液中滴加氢氧化钠溶液的反应的离子方程式:_____________。
②写出能用离子方程式CO32-+2H+=CO2↑+H2O表示的一个化学方程式:__________。
【答案】②③⑤⑥⑧ ④⑨ ①⑦⑧⑩ NaHSO4=Na++H++SO42- Al2(SO4)3=2Al3++3SO42- NH4NO3=NH4++NO3- Cu2++2OH-==Cu(OH)2↓ Na2CO3+2HCl=2NaCl+CO2↑+H2O(或其他)
【解析】
(1)在水溶液里或熔化状态下能够自身电离出离子的化合物是电解质,属于电解质的是NaCl晶体、NaHSO4、CaO、HCl、熔融Ba(OH)2,答案选②③⑤⑥⑧;在水溶液里和熔融状态下都不能自身电离出离子的化合物是非电解质,属于非电解质的是CO2、C2H5OH,答案选④⑨;含有自由移动电子或离子的物质可以导电,能导电的是Cu、稀H2SO4、熔融Ba(OH)2、NaCl溶液,答案选①⑦⑧⑩;(2)①NaHSO4在水溶液中的电离方程式为NaHSO4=Na++H++SO42-;②Al2(SO4)3在水溶液中的电离方程式为Al2(SO4)3=2Al3++3SO42-;③NH4NO3在水溶液中的电离方程式为NH4NO3=NH4++NO3-。(3)①硫酸铜溶液中滴加氢氧化钠溶液生成氢氧化铜沉淀和硫酸钠,反应的离子方程式为Cu2++2OH-==Cu(OH)2↓:②能用离子方程式CO32-+2H+=CO2↑+H2O表示的一个化学方程式可以是Na2CO3+2HCl=2NaCl+CO2↑+H2O。
点睛:化合物在水溶液中或受热熔化时本身能否发生电离是区别电解质与非电解质的理论依据,能否导电则是实验依据。因此能导电的物质不一定是电解质,如石墨;电解质本身不一定能导电,如NaCl晶体。
【题型】填空题
【结束】
27
【题目】为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色A________,B____________。
(2)写出上述过程中有关反应的化学方程式:
Fe2O3→A_______________________;A→B____________________________。
(3)B→C可看到的现象是___________________________________________。
(4)将A的饱和溶液滴入沸水中并不断加热,可制得_______________胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为___________效应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的二氧化硫和含0.7 mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应2SO2+O2![]() 2SO3。反应达到平衡后,将容器中的混合气体通过过量氢氧化钠溶液,气体体积减小了21.28 L;再将剩余气体通过一种碱性溶液吸收氧气,气体的体积又减少了5.6 L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)请回答下列问题:
2SO3。反应达到平衡后,将容器中的混合气体通过过量氢氧化钠溶液,气体体积减小了21.28 L;再将剩余气体通过一种碱性溶液吸收氧气,气体的体积又减少了5.6 L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)请回答下列问题:
(1)判断该反应达到平衡状态的标志是(填字母)__________________。
a.二氧化硫和三氧化硫浓度相等
b.三氧化硫百分含量保持不变
c.容器中气体的压强不变
d.三氧化硫的生成速率与二氧化硫的消耗速率相等
e.容器中混合气体的密度保持不变
(2)求该反应达到平衡时,消耗二氧化硫的物质的量占原二氧化硫的物质的量的百分比____。
(3)若将平衡混合气体的5%通入过量的氯化钡溶液中,生成沉淀的质量是多少?______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-VOCl2电池是一种基于阴离子传导的新型二次电池,其简化装置示意图如下。总反应为Mg+2VOCl2![]() MgCl2+2VOCl,下列说法错误的是
MgCl2+2VOCl,下列说法错误的是
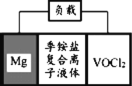
A.采用Mg作电极材料比Li的安全性更高
B.放电时正极反应为VOCl2+e=VOCl+Cl
C.放电过程中Cl穿过复合离子液体向Mg移动
D.为该电池充电时Mg电极应与电源的正极相连
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com