
分析 (1)能导电的物质:必须具有能自由移动的带电的微粒,金属能导电--是由于金属中存在能自由移动的带负电的电子.
非电解质是指:在熔融状态和水溶液中都不能导电的化合物;单质,混合物既不是电解质也不是非电解质;
强电解质是在水溶液中或熔融状态下能完全电离的电解质,包括强酸、强碱、活泼金属氧化物和大部分盐;弱电解质是在水溶液中不能完全电离的电解质,包括弱酸、弱碱、水等;
(2)NaHCO3是强电解质,在水溶液里完全电离生成钠离子和碳酸氢根离子;
(3)碳酸氢钠和醋酸反应生成醋酸钠和水、二氧化碳;
(4)将物质⑥碳酸氢钠固体配制成溶液,逐滴加入⑦氢氧化钡溶液,溶液中至沉淀量最大生成碳酸钡沉淀.
解答 解:(1)①石墨、②铝存在能自由移动的带负电的电子能导电; ④氨水; ⑦氢氧化钡溶液,有能自由移动的阴、阳离子,能导电;
非电解质是在水溶液中或熔融状态下都不能能够导电的化合物,酒精和二氧化碳符合;
强电解质是在水溶液中或熔融状态下能完全电离的电解质,包括强酸、强碱、活泼金属氧化物和大部分盐,⑥碳酸氢钠固体、⑨氧化钠固体、⑩氯化氢气体都是强电解质;弱电解质是在水溶液中不能完全电离的电解质,包括弱酸、弱碱、水等,冰醋酸是弱电解质;
故答案为故答案为:①②④⑦;③⑤;⑥⑨⑩;⑧;
(2)碳酸氢钠为强电解质,完全电离,电离方程式为:NaHCO3=Na++HCO3-,
故答案为:NaHCO3=Na++HCO3-;
(3)碳酸氢钠和醋酸反应生成醋酸钠和水、二氧化碳,反应离子方程式为:HCO3-+CH3COOH=CH3COO-+H2O+CO2↑
故答案为:HCO3-+CH3COOH=CH3COO-+H2O+CO2↑;
(4)将物质⑥碳酸氢钠固体配制成溶液,逐滴加入⑦氢氧化钡溶液,溶液中至沉淀量最大生成碳酸钡沉淀,反应的离子方程式为:Ba2++OH-+HCO3-=BaCO3↓+H2O,
故答案为:Ba2++OH-+HCO3-=BaCO3↓+H2O.
点评 本题重点考查了电解质、非电解质概念的辨析、强、弱电解质的判断、离子反应等,抓住电解质必须是化合物,抓住弱电解质的特征“部分电离”,强电解质”在水溶液中或熔融状态下,能完全电离”是解答本题的关键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 水、硝酸银溶液、稀硝酸 | B. | 水、氢氧化钠溶液、盐酸 | ||
| C. | 水、氢氧化钾溶液、盐酸 | D. | 水、氢氧化钾溶液、硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某学生为了使过滤操作能自动添加液体,设计了“自动加液过滤器”如图所示,在倒置的烧瓶中盛放待过滤的液体,液体从“液体流出管”流入漏斗,为使液体顺利流下,还需插入“空气导入管”与大气相通,“空气导入管”下口应在( )
某学生为了使过滤操作能自动添加液体,设计了“自动加液过滤器”如图所示,在倒置的烧瓶中盛放待过滤的液体,液体从“液体流出管”流入漏斗,为使液体顺利流下,还需插入“空气导入管”与大气相通,“空气导入管”下口应在( )| A. | 滤纸边沿下方 | B. | 滤纸边沿上方 | ||
| C. | 待过滤液液面上方 | D. | 待过滤液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把a L0.1mol•L-1的CH3COOH溶液与bL 0.1mol•L-1的KOH溶液混合,所得溶液中一定存在:c(K+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | 把0.1mol•L-1的NaHCO3溶液与0.3mol•L-1的Ba(OH)2溶液等体积混合,所得溶液中一定存在:c(OH-)>c(Ba2+)>c(Na+)>c(H+) | |
| C. | 向1mol•L-1的CH3COOH溶液中加入少量CH3COONa固体,由于CH3COONa水解显碱性,所以溶液的pH升高 | |
| D. | 常温下,在pH=3的CH3COOH溶液和pH=11的NaOH溶液中,水的电离程度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将金属钠保存在煤油中 | |
| B. | 少量的白磷可保存在水中 | |
| C. | 纯碱溶液用带磨口玻璃瓶塞的试剂瓶保存 | |
| D. | 硝酸银溶液盛放在棕色试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若将四种溶液稀释100倍,溶液pH大小顺序:③>④>①>② | |
| B. | ③和④分别用等浓度的硫酸溶液中和,消耗硫酸溶液的体积:③=④ | |
| C. | ①与②分别与足量镁粉反应,生成H2的量:①<② | |
| D. | ②和③混合,所得混合溶液的pH大于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
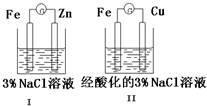
| A. | Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-═4OH- | |
| B. | Ⅰ和Ⅱ中负极反应均是Fe-2e-═Fe2+ | |
| C. | Ⅰ和Ⅱ中正极均被保护 | |
| D. | Ⅰ和Ⅱ中分别加入少量K3[Fe(CN)6]溶液,均有蓝色沉淀产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com