
b a |
b a |
| A、此气体分子中含有的中子数为b-a | ||
| B、此元素的离子中含有的电子数为a+n | ||
| C、此气体分子中含有的质子数为c(a+n) | ||
D、一个该同位素原子的质量约为
|
b a |
| b |
| 6.02×1023 |


科目:高中化学 来源: 题型:
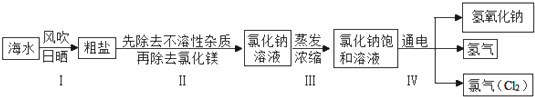

| 阴离子 阳离子 | OH- | CO
| ||
| Ca2+ | 微 | 不 | ||
| Mg2+ | 不 | 微 |
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取一定量的氯化钠溶液于试管中,加入适量的NaOH溶液 | 无明显现象 | 说明MgCl2 |
| 步骤二:往步骤一所得溶液中加入适量的 | 产生白色沉淀 | 说明溶液中含有CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(HCO3)2溶液中滴入过量 NaOH 溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| B、向NaAlO2 溶液中通人过量的 C02:CO2+2H20+A102-═Al(OH)3↓+HCO3- |
| C、0.01mol/L NH4Al(SO4)2 溶液与 O.02mol/L Ba(OH)2溶液等体积混合:Al3++2S042-+2Ba2++40H-═2BaSO4↓+AlO2-+2H20 |
| D、向Ca(ClO)2溶液中通入过量的 SO2:C10-+SO2+H2O═HClO+HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5mol/L |
| B、0.8mol/L |
| C、1mol/L |
| D、1.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AgNO3 |
| B、HCl |
| C、NaOH |
| D、NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
 与NaOH的水溶液共热的化学方程式为
与NaOH的水溶液共热的化学方程式为
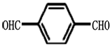 )的氧化产物“对苯二甲酸”与“乙二醇”发生缩聚,生成的聚酯纤维(涤纶)的结构简式为
)的氧化产物“对苯二甲酸”与“乙二醇”发生缩聚,生成的聚酯纤维(涤纶)的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 序号 | 时间 浓度 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| ① | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| ② | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| ③ | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| ④ | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4和C4H6 1:1 |
| B、CH4和C4H10 5:1 |
| C、C3H4和C3H8 3:1 |
| D、C2H2和C4H8 任意比 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com