
| A. | ②③⑤ | B. | ②④ | C. | ①③④ | D. | ①②③④⑤ |
分析 从两个角度考虑,一是可逆反应,二是物质的性质与浓度有关,例如某些酸在浓度较大时具有较强的氧化性或还原性,当浓溶液时可以发生反应,但随着反应的消耗,变成稀溶液往往就不具备继续反应的性质.
解答 解:①锌不论与浓硫酸还是稀硫酸都能反应,一种物质过量时,另一种能完全反应,故①错误;
②浓盐酸反应到最后变成稀盐酸了,无法完全反应,浓盐酸中H+和Cl-的浓度大,还原性强,在加热条件下能被MnO2氧化,生成Cl2,随反应进行,H+和Cl-的浓度逐渐减小,还原性逐渐减弱,当达到一定程度时,MnO2就不可以氧化Cl-了,因此二氧化锰和稀盐酸不会反应,故②正确;
③随反应进行浓硫酸变为稀硫酸,铜无法与稀硫酸反应,无论铜怎么过量,都不能完全消耗完硫酸,故③正确;
④Ag与稀硝酸能反应,硝酸过量时,Ag能完全反应,故④错误;
⑤稀硫酸与块状石灰石反应生成微溶物硫酸钙,附着在碳酸钙表面阻止反应的进一步发生,故⑤正确;
故选A.
点评 本题考查物质的性质,难度不大,注意化学反应中的一些特殊情况,本题的可逆性和浓度问题.


科目:高中化学 来源: 题型:选择题
| A. | 6.4gO2和O3的混合气体,含氧原子数为0.4NA | |
| B. | 分子标准状况下,11.2LCCl4中含分子数为0.5NA | |
| C. | 1mol乙酸(忽视挥发损失)与足量的C2H518OH在浓硫酸作用下加热,充分反应可生成NA个CH3CO18OC2H5 | |
| D. | 常温常压下,7.8gNa2O2含离子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,2.24 L SO2与O2混合气体中所含氧原子数小于0.2NA | |
| B. | 点解饱和食盐水时,当溶液pH由7变为13,电路中转移的电子数为0.1NA | |
| C. | 常温下,1 L pH=13的Ba(OH)2中含有的OH-数目为0.2NA | |
| D. | 10 mL 98%的H2SO4溶液,加入水中稀释至100 mL,H2SO4的质量分数为9.8% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2 | B. | NO | C. | N2O | D. | N2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某温度时的混合溶液中c(H+)=$\sqrt{{K}_{W}}$mol•L-1,说明该溶液呈中性(Kw为该温度时水的离子积常数) | |
| B. | 由水电离出的c(H+)=10-12mol•L-1的溶液中:Na+、Ba2+、HCO3-、Cl-可以大量共存 | |
| C. | 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12.向含有Cl-、CrO42-且浓度均为0.010 mol•L-1溶液中逐滴加入0.010 mol•L-1的AgNO3溶液时,CrO42-先产生沉淀 | |
| D. | 常温下pH=7的CH3COOH和NaOH混合溶液中,c(Na+)>c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
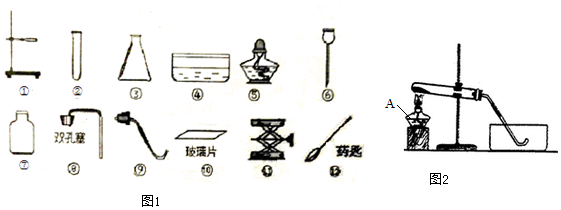
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于10 s | B. | 等于15 s | C. | 大于15 s | D. | 小于15 s |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液甲的pH>7 | |
| B. | 对溶液甲进行微热,K1、K2同时增大 | |
| C. | 溶液甲中,c(Na+)+c(H+)=c(CH3COO-) | |
| D. | 若在溶液甲中加入5 mL 0.1 mol•L-1的盐酸,则溶液中醋酸的K1会变大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com