
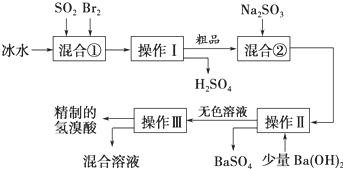
分析 Br2具有强氧化性,在溶液中将SO2氧化为H2SO4,反应室1中发生反应:SO2+Br2+2H2O=H2SO4+2HBr,Br2氧化SO2放出很多热量,液溴、氢溴酸易挥发,反应室①使用冰水降低温度,防止Br2和HBr挥发,操作I是将互溶的硫酸、氢溴酸分离,而氢溴酸易挥发,应采取蒸馏进行分离.粗品中可能含有挥发出的Br2,加入Na2SO3,除去粗品中未反应完的溴,再加入氢氧化钡溶液,使反应生成SO42- 转化硫酸钡沉淀,再进行过滤分离,无色溶液中含有HBr及NaBr,再蒸馏得到精致的氢溴酸.
(1)Br2具有强氧化性,在溶液中将SO2氧化为H2SO4,自身被还原为HBr;
(2)Br2氧化SO2放出很多热量,液溴、氢溴酸易挥发;
(3)操作Ⅱ分离固体与液体,应是过滤,操作Ⅲ是将互溶的硫酸、氢溴酸分离,而氢溴酸易挥发;
(4)粗品中可能含有挥发出的Br2,加入Na2SO3,还原除去粗品中的Br2 ;
(5)用KSCN溶液检验Fe3+,滴加KSCN溶液,溶液变成血红色;由工艺流程可知,溶液中可能含有Br2,可以用CCl4萃取方法检验.
解答 解:Br2具有强氧化性,在溶液中将SO2氧化为H2SO4,反应室1中发生反应:SO2+Br2+2H2O=H2SO4+2HBr,Br2氧化SO2放出很多热量,液溴、氢溴酸易挥发,反应室①使用冰水降低温度,防止Br2和HBr挥发,操作I是将互溶的硫酸、氢溴酸分离,而氢溴酸易挥发,应采取蒸馏进行分离.粗品中可能含有挥发出的Br2,加入Na2SO3,除去粗品中未反应完的溴,再加入氢氧化钡溶液,使反应生成SO42- 转化硫酸钡沉淀,再进行过滤分离,无色溶液中含有HBr及NaBr,再蒸馏得到精致的氢溴酸.
(1)Br2具有强氧化性,在溶液中将SO2氧化为H2SO4,自身被还原为HBr,反应室1中发生反应:SO2+Br2+2H2O=H2SO4+2HBr,
故答案为:SO2+Br2+2H2O=H2SO4+2HBr;
(2)Br2氧化SO2放出很多热量,液溴、氢溴酸易挥发,反应室①使用冰水降低温度,防止Br2和HBr挥发,
故答案为:降低体系温度,防止Br2和HBr挥发,使反应进行完全;
(3)操作Ⅱ分离固体与液体,应是过滤,操作Ⅲ是将互溶的硫酸、氢溴酸分离,而氢溴酸易挥发,应采取蒸馏进行分离,
故答案为:过滤;蒸馏;
(4)粗品中可能含有挥发出的Br2,加入Na2SO3,还原除去粗品中的Br2,
故答案为:除去粗产品中未反应完的溴;
(5)用KSCN溶液检验Fe3+:取少许溶液滴加KSCN溶液,溶液变成血红色,说明氢溴酸呈淡黄色是因为含Fe3+,由工艺流程可知,溶液中可能含有Br2,可以用CCl4萃取方法检验:用胶头滴管取制得的氢溴酸于试管中,滴加CCl4、振荡、静止分层,下层呈橙红色,说明氢溴酸呈淡黄色是因为含Br2,用于证明该假设所用的试剂为CCl4,
故答案为:KSCN溶液,溶液变成血红色,含有Br2,CCl4;
点评 本题以制备氢溴酸为载体,考查学生对工艺流程的理解、物质的分离提纯等基本操作、离子检验、物质性质等,难度中等,是对知识的综合运用,需学生具有扎实的基础知识与灵活运用知识解决问题的能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
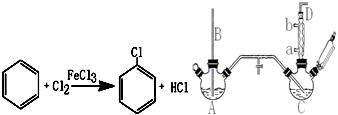
| 名称 | 相对分子质量 | 沸点/(℃) | 密度/(g/mL) |
| 苯 | 78 | 78 | 0.88 |
| 氯苯 | 112.5 | 132.2 | 1.1 |
| 邻二氯苯 | 147 | 180.4 | 1.3 |

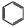 +2HCl+O2$→_{210℃}^{催化剂}$2
+2HCl+O2$→_{210℃}^{催化剂}$2 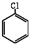 +2 H2O.
+2 H2O.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 已知:乙醇、1,2-二溴乙烷、乙醚的有关物理性质如下表所示
已知:乙醇、1,2-二溴乙烷、乙醚的有关物理性质如下表所示| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 通常状况下的状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 熔点/℃ | -130 | 9 | -116 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
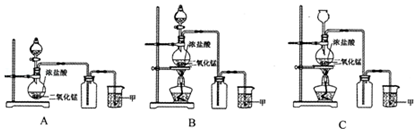
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com