
【题目】按照第一电离能由大到小的顺序排列错误的是( )
A. Be、Mg、Ca B. Na、Mg、Al C. He、Ne、Ar D. Li、Na、K
【答案】B
【解析】同周期从左到右元素的第一电离能呈增大趋势,第IIA族大于第IIIA族,第VA族大于第VIA族;同主族从上到下元素的第一电离能逐渐减小。
A项,Be、Mg、Ca都是第IIA族元素,核电荷数依次增大,同主族从上到下元素的第一电离能逐渐减小,第一电离能按Be、Mg、Ca的顺序减小;B项,Na、Mg、Al都是第三周期元素,核电荷数依次增大,根据同周期从左到右元素的第一电离能呈增大趋势,Mg的价电子排布为3s2,处于全充满较稳定,第一电离能Mg![]() Al
Al![]() Na;C项,He、Ne、Ar都是0族元素,核电荷数依次增大,同主族从上到下元素的第一电离能逐渐减小,第一电离能按He、Ne、Ar的顺序减小;D项,Li、Na、K都是第IA族元素,核电荷数依次增大,同主族从上到下元素的第一电离能逐渐减小,第一电离能按Li、Na、K的顺序减小;按第一电离能由大到小的顺序排列错误的是B项,答案选B。
Na;C项,He、Ne、Ar都是0族元素,核电荷数依次增大,同主族从上到下元素的第一电离能逐渐减小,第一电离能按He、Ne、Ar的顺序减小;D项,Li、Na、K都是第IA族元素,核电荷数依次增大,同主族从上到下元素的第一电离能逐渐减小,第一电离能按Li、Na、K的顺序减小;按第一电离能由大到小的顺序排列错误的是B项,答案选B。


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 石灰乳与过量碳酸氢钙溶液反应:HCO3—+Ca2++OH-==CaCO3↓+H2O
B. 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O(沸水)![]() Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
C. 二氧化碳通入足量的氢氧化钠溶液:CO2 + OH-═ HCO3-
D. 氧化钠与盐酸反应:O2-+2H+ ==== H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁有两种氯化物,都是重要的化工试剂,一些性质及制备方法如下:
氯化铁:熔点306℃,沸点315℃,易吸收空气中的水分而潮解。工业上采用向500600℃的铁粉中通入氯气来生产无水氯化铁。
氯化亚铁:熔点670℃, 易升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。实验室可用下图所示的装置模拟工业生产无水氯化铁,请回答相关问题。

(1)装置A用于KMnO4固体与浓盐酸反应制氯气,反应的离子方程式为______________。
(2)弯曲的a管所起的作用是_____________________;装置采用较粗的导管来连接装铁粉的硬质玻璃管和广口瓶C,其目的是_____________________________________。
(3)导管b 口应与_______________ (从虚线框装置中选择装置的字母序号)连接,这样可避免反应系统与环境间的相互影响。
(4)实验完成后,取广口瓶C中收集到的产物进行如下测定
①称取4.52g样品溶于过量的稀盐酸中:②加入足量H2O2;③再加入足量NaOH溶液:④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。则该样品中Fe元素的质量分数为______%。
(5)由上分析数据和计算得出结论:
①用此装置制得的无水氯化铁含铁_________偏高,偏低),显然其中含有较多________的杂质。
②若要得到较纯净的无水氯化铁,可采取的装置改进措施是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G、H、I九种物质,其中A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G、F是单质,其余均为化合物,H是一种淡黄色固体,它们的转化关系如图所示。请回答:
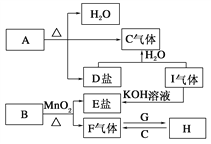
(1)画出G离子结构示意图________;
(2)写出B、I的化学式B________,I________;
(3)写出H的一种用途__________________________________;
(4)写出A受热分解的化学方程式_________________________;
(5)若10g的C6H12O6在氧气中充分燃烧,将产物全部与足量的H充分反应,反应后固体增重____________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1x105Pa和298 K时,将1 mol气态AB分子分离成气态A原子和B原子所需要的能量称为A-B共价键的键能( kJ/mol)。下面是一些共价键的键能(已知氨分子中有3个等价的氮氢共价键):
共价键 | H-H | N≡N | N-H |
键能(kJ/mol) | 436 | 945 | 391 |
(1)根据上表中的数据判断工业合成氨的反应、N2(g)+3H2(g)![]() 2NH3(g)是____(填“吸热”或“放热”)反应。
2NH3(g)是____(填“吸热”或“放热”)反应。
(2)在298 K时,取1mol氮气和3mol氢气放入一密闭容器中,若在催化剂存在下两者恰好完全反应.理论上放出或吸收的热量为Q1,Q1的数值是____。
(3)实际生产中,放出或吸收的热量为Q2,下列选项正确的是____(填选项代号)。
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2
你作出此选择的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中含有的阳离子为H+、Na+、Mg2+、Al3+、Ba2+中的一种或几种,向该溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此确定原溶液中一定含有的阳离子是

A. Mg2+、Al3+、Na+ B. H+、Mg2+、Al3+ C. H+、Ba2+、Al3+ D. Ba2+、Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在铜与稀HNO3的反应中,若有lmol HNO3被还原,则参加反应的铜的物质的量为
A. 8/3mol B. 3/8mol C. 3/2mol D. 3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、油脂和蛋白质是生命活动所必需的营养物质。下列叙述正确的是
A.淀粉水解的最终产物是葡萄糖
B.葡萄糖能发生氧化反应和水解反应
C.植物油不能发生水解反应,植物油属于高分子化合物
D.蛋白质遇浓硫酸变为黄色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com