
分析 (1)根据NaCl不能和盐酸反应而和Na2CO3能与盐酸反应来鉴别;
(2)碳酸氢钠可与NaHCO3反应生成碳酸钠和水;
(3)氧化铝与氢氧化钠溶液反应,而氧化镁不反应,据此可除去氧化镁中混有的氧化铝.
解答 解:(1)因NaCl不能和盐酸反应,Na2CO3能与盐酸反应生成氯化钠、水、二氧化碳,所以鉴别NaCl溶液和Na2CO3的试剂是盐酸,反应的离子方程式为:CO32-+2H+=CO2↑+H2O,
故答案为:盐酸;CO32-+2H+=CO2↑+H2O;
(2)Na2CO3不与氢氧化钠溶液反应,而NaHCO3与氢氧化钠溶液反应生成碳酸钠和水,反应的离子方程式为:HCO3-+OH-=H2O+CO32-,
故答案为:NaOH溶液;HCO3-+OH-=H2O+CO32-;
(3)MgO不与NaOH溶液反应,而氧化铝与氢氧化钠溶液反应,据此除去MgO中少量Al2O3杂质,反应的离子方程式为:Al2O3+2OH-=2AlO2-+H2O,
故答案为:NaOH溶液:Al2O3+2OH-=2AlO2-+H2O.
点评 本题考查离子反应方程式书写及除杂,为高频考点,题目难度不大,把握物质的性质差异及及发生的离子反应为解答的关键,侧重混合物分离提纯及离子反应的考查.


科目:高中化学 来源: 题型:多选题
 | ① | ② | ③ | ④ | ⑤[ | ⑥ | ⑦ | ⑧ |
| 原子半径/10-10m | 0.66 | 1.36 | 1.23 | 1.10 | 0.99 | 1.54 | 0.70 | 1.18 |
| 最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 负化合价 | -2 | -3 | -1 | -3 |
| A. | 元素①⑧形成的化合物具有两性 | |
| B. | 元素⑦位于第二周期Ⅴ族 | |
| C. | 元素④⑤形成的化合物是离子化合物 | |
| D. | 元素⑥的最高价氧化物对应水化物碱性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食盐水、牛奶、豆浆 | B. | 碘酒、泥水、血液 | ||
| C. | 白糖水、食盐水、茶叶水 | D. | Ca(OH)2悬浊液、澄清石灰水、石灰浆 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高锰酸钾溶液和双氧水可用于消毒都是利用了其强氧化性 | |
| B. | 乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 | |
| C. | 乙醇能使蛋白质变性,故不能用于人体皮肤的消毒 | |
| D. | 在次氯酸钠溶液中通入少量二氧化硫可得到亚硫酸钠和次氯酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
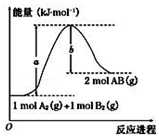
| A. | 每生成 2 个分子 AB 吸收(a-b) kJ 热量 | |
| B. | 该反应热△H=+(a-b)kJ•mol-1 | |
| C. | 逆反应的活化能高于正反应的活化能 | |
| D. | 断裂1mol A-A 和 1mol B-B 键,放出 a kJ 能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
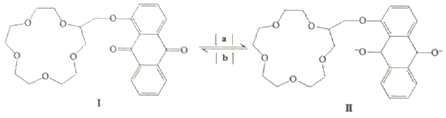
| A. | 物质Ⅰ的分子式是C25H28O8 | B. | 反应是氧化反应 | ||
| C. | 1molⅠ可与8molH2发生加成反应 | D. | 物质Ⅰ的所有原子不可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y与T形成的化合物中含有离子键 | |
| B. | X、Z、T对应的简单离子半径由大到小的顺序为T>X>Z | |
| C. | 1 mol Z的单质与足量X的单质反应,转移电子物质的量可能是2 mol,也可能是1 mol | |
| D. | X与Y形成的共价化合物XY2不能溶于强碱溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com