


科目:高中化学 来源: 题型:
| 元素代号 | L | X | R | T |
| 原子半径/nm | 0.191 | 0.102 | 0.154 | 0.074 |
| 主要化合价 | +1 | +6、-2 | +1 | -2 |
| A、L单质的熔点比R单质的高 |
| B、T对应的氢化物的沸点比X对应的氢化物高 |
| C、R单质在氧气中燃烧生成R2O2 |
| D、L、X形成的简单离子核外电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
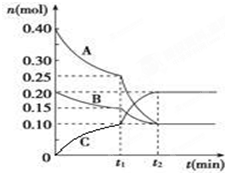 现将0.4mol A气体和0.2mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量随时间的变化如图:
现将0.4mol A气体和0.2mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量随时间的变化如图:查看答案和解析>>
科目:高中化学 来源: 题型:
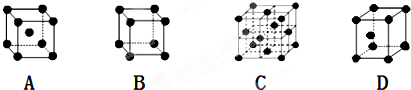
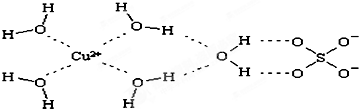
 是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为
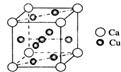
是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为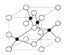 是铜的某种氧化物的晶胞结构示意图,该晶体的密度为a g/cm3,设阿伏伽德罗常数的值为NA,则该晶胞的体积为
是铜的某种氧化物的晶胞结构示意图,该晶体的密度为a g/cm3,设阿伏伽德罗常数的值为NA,则该晶胞的体积为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com