
【题目】用98%的浓硫酸(ρ=1.84g/cm3)配制250mL 1mol/L的稀硫酸,所需浓硫酸的体积为mL(小数点后保留一位有效数字).如果实验室有10mL、20mL、50mL量筒,应选用mL量筒,实验中还需要用到的仪器有烧杯、胶头滴管、玻璃棒和 .
科目:高中化学 来源: 题型:
【题目】如图图示与对应的叙述相符的是( ) 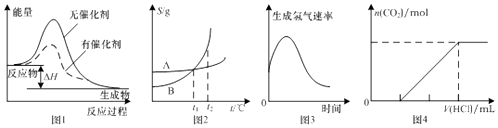
A.图1表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图2表示A,B两物质的溶解度随温度变化情况,将t1℃时A,B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A
C.图3表示镁条放入盐酸中生成氢气速率随时间的变化,起初反应速率加快的原因可能是该反应为放热反应
D.图4表示在含等物质的量NaOH,Na2CO3的混合溶液中滴加0.1 molL﹣1盐酸至过量时,产生气体的体积与消耗盐酸的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)由乙烯制取聚乙烯的化学方程: .
(2)写出下列物质的结构简式; ①2,3﹣二甲基戊烷
②3﹣甲基﹣2﹣戊烯
③间二甲苯
(3)分子中含有5个碳原子的链状单炔烃的分子式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关生活中化学的叙述中,正确的是
A.只用米汤就能检验出食盐中是否加碘
B.可用热的纯碱溶液清洗油污
C.“光化学烟雾”的形成与二氧化硫有关
D.用硅单质制光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在浓CaCl2溶液中通入NH3和CO2 , 可以制得纳米级碳酸钙(粒子直径在1~100nm之间).图1所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请你一起参与实验并根据要求回答有关问题: 
(1)实验室制取、收集干燥的NH3 , 需选用上述仪器装置的接口连接顺序是(选填字母):a接 , 接 , 接h;用A装置制取NH3的化学反应方程式为: .
(2)用图2所示装置也可以制取NH3 , 则圆底烧瓶中的固体可以选用(选填字母编号).
A.碱石灰
B.生石灰
C.无水氯化钙
D.无水硫酸铜
E.烧碱
(3)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是;试写出制纳米级碳酸钙的化学方式 .
(4)请设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析实验中出现下列现象对所配溶液的浓度有何影响:
(1)①浓硫酸溶解后未冷却至室温即转移至容量瓶中进行定容,(填“偏高”、“偏低”或“无影响”);
②定容时仰视刻度线,;填“偏高”、“偏低”或“无影响”);
③量取好浓硫酸倒入烧杯溶解后,用水洗涤量筒2~3次,将洗涤液倒入烧杯中, . (填“偏高”、“偏低”或“无影响”);
(2)7.8g镁铝合金与足量的稀盐酸反应,生成氢气的体积为8.96L(标准状况),则此反应中转移电子的数目为 , 镁和铝分别产生氢气的体积之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下面每一小题.
(1)除去乙烷中混有的少量乙烯,所用的试剂是;
(2)除去混在硝基苯中的硝酸,所用的试剂是;
(3)![]() 的一氯取代物有种
的一氯取代物有种
(4)2,3﹣二甲基﹣4﹣乙基已烷 (写出结构简式) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
(1)常温下,工业上用铁质容器盛放冷的浓硫酸,其原因是 .
(2)称取碳素钢6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y. ①甲同学认为X中除Fe3+之外还可能含有Fe2+ . 若要确认其中的Fe2+ , 应选用(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此可求算气体Y中SO2的体积分数 .
写出探究②中出现的所有离子反应方程式 .
(3)根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893gL﹣1 . 为此设计了下列探究实验装置(图中夹持仪器省略,假设有关气体完全反应). 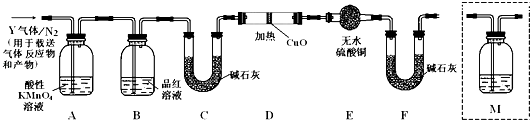
装置B中试剂的作用是 .
(4)分析Y气体中的Q2气体是如何生成的 . (用化学方程式表示).
(5)为确认Q2的存在,需在装置中添加洗气瓶M于(选填序号). a.A之前 b.A﹣B间 c.B﹣C间 d.C﹣D间
(6)如果气体Y中含有Q1 , 预计实验现象应是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com