
| A、500mL2mol?L-1稀硫酸 |
| B、150mL5mol?L-1稍酸 |
| C、50mL3mol?L-1盐酸 |
| D、500mL2mol?L-1稀硫酸和少量硫酸铜 |
 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
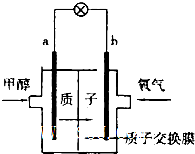 某研究性学习小组为了证明某酸HmA是强酸还是弱酸,设计了如下实验方案,请回答有关问题:
某研究性学习小组为了证明某酸HmA是强酸还是弱酸,设计了如下实验方案,请回答有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=7的溶液 |
| B、c(H+)=c(OH-)=10-6mol/L溶液 |
| C、由强酸、强碱等物质的量反应后得到的溶液 |
| D、滴入甲基橙指示剂显橙色的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢管与铜管家露天堆放在一起,钢管不易腐蚀 |
| B、生铁浸泡在食盐水中发生析氢腐蚀 |
| C、给铁钉镀铜可采用CuSO4作电镀液 |
| D、电解饱和食盐水时在阳极得到氯气,阴极得到金属钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性:H3PO4>HNO3>HClO4 |
| B、稳定性:HF>H2O>NH3 |
| C、微粒半径:F->Na+>Mg2+ |
| D、碱性:KOH>NaOH>Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当△H<O时,表示该反应为吸热反应 | ||
B、已知C(s)+
| ||
| C、反应热的大小与反应物所具有的能量和生成物所具有的能量无关 | ||
| D、化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、铝粉投入到NaOH溶液中:Al+2OH-═AlO2-+H2↑ |
| C、氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+ |
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
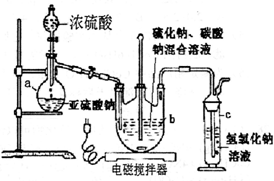 硫代硫酸钠(Na2S2O3?5H2O)俗名“大苏打”,又称为“海波”.它易溶于水,难溶于乙醇,加热易分解.工业上常用亚硫酸钠法、硫化碱法等制备.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:实验具体操作步骤为:
硫代硫酸钠(Na2S2O3?5H2O)俗名“大苏打”,又称为“海波”.它易溶于水,难溶于乙醇,加热易分解.工业上常用亚硫酸钠法、硫化碱法等制备.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:实验具体操作步骤为:| 实验序号 | 1 | 2 | 3 |
| N2aS2O3溶液体积(mL) | 19.8 | 20.02 | 21.18 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com