
实验室制取的乙烯常含有少量二氧化硫,现设计如下实验,确认混合气体中有乙烯和二氧化硫。

(1)a、b、c、d装置可盛放的试剂是:a________,b______,c_____,d______。
A.品红溶液 B.NaOH溶液C.浓硫酸 D.酸性高锰酸钾溶液
(2)确定含有乙烯的现象是_________________________________________________。
【答案】 (1)A B A D
c装置中品红溶液不褪色,d装置中酸性高锰酸钾溶液褪色
【解析】试题分析:二氧化硫的检验用品红溶液,乙烯的检验用高锰酸钾酸性溶液,乙烯和二氧化硫都能使高锰酸钾酸性溶液褪色,所以先检验二氧化硫,然后检验乙烯,同在检验乙烯之前用NaOH溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净,最后用高锰酸钾酸性溶液褪色检验乙烯。
(1)因装置①用来检验SO2,试管中品红溶液褪色,说明含有SO2,装置②试管装有NaOH溶液除去SO2,装置③试管通过品红溶液不褪色确认SO2已除干净,装置④通过高锰酸钾酸性溶液褪色检验乙烯,故答案为:①A;②B;③A;④D;
(2)c装置中品红溶液不褪色,d装置中酸性高锰酸钾溶液褪色。
考点:乙烯的实验室制法
点评:本题主要考查了实验室制乙烯产物的检验,当有多种产物需检验时,应考虑先后顺序,在除去杂质气体时不能引入新杂质。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
常温下0.1 mol·L-1氨水的pH=a,下列能使溶液pH=(a+1)的措施是
A.加入适量的氢氧化钠固体 B.将溶液稀释到原体积的 10倍
C.加入等体积0.2 mol·L-1氨水 D.降低溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示。有关说法不正确的是( )
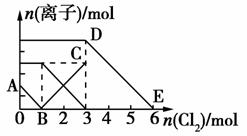
A.线段BC代表Fe3+物质的量的变化情况
B.原混合溶液中n(FeBr2)=3 mol
C.当通入2 mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-
D.原溶液中n(Fe2+):n(I-):n(Br-)=3:1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
将含O2和CH4的混合气体充入装有23.4gNa2O2的密闭容器中,点火花点燃,反应结束后,容器温度为150℃、压强为0 Pa。将残留物溶于水,无气体逸出。下列叙述正确的是( )
A.原混合气体中O2和CH4的体积比为2∶1;
B.原混合气体中O2和CH4的体积比为1∶2;
C.残留固体中有Na2CO3和NaOH;
D.残留固体中只有Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.淀粉和蛋白质均可作为生产葡萄糖的原料
B.实验室可用酸性高锰酸钾溶液鉴别甲苯和己烯
C.石油裂化和油脂皂化都是高分子生成小分子的过程
D.装饰材料中的甲醛和芳香烃会造成居室污染
查看答案和解析>>
科目:高中化学 来源: 题型:
随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。
(1)有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A、CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0kJ/mol
B、CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-192.9kJ/mol
又知H2O(l)=H2O(g) ΔH=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式 。
(2)下图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图。甲醇在催化剂作用下提供质子和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O。则c电极是 (填“正极”或“负极”),
c电极上发生的电极反应式是 。

查看答案和解析>>
科目:高中化学 来源: 题型:
科学家将两种元素铅和氪的原子核对撞,获得了一种质子数为118、质量数为293的超重元素,该元素原子核内的中子数与核外电子数之差为
A.47 B.57
C.61 D.175
查看答案和解析>>
科目:高中化学 来源: 题型:
臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)  N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的 判断正确的是
判断正确的是
| A | B | C | D |
|
|
|
|
|
| 升高温度,平衡常数减小 | 0~3s内,反应速率为: v(NO | t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,11.2LCH2Cl2中含有的分子数为0.5NA
B.2.3g钠与足量氧气反应,转移的电子数为0.1 NA
C.1 mol甲基中含有的电子数为10NA
D.2.7g铝与足量氢氧化钠溶液反应转移的电子数NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com