
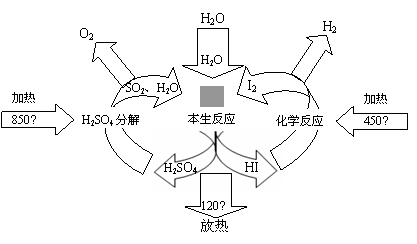
 氢能是一种绿色能源,一种目前成熟的方法是利用碘硫热化学循环制备氢气,其原理示意图如下。
氢能是一种绿色能源,一种目前成熟的方法是利用碘硫热化学循环制备氢气,其原理示意图如下。
(1)已知:SO3(g)  SO2(g)+1/2O2(g) △H1 =-98.3kJ·mol-1
SO2(g)+1/2O2(g) △H1 =-98.3kJ·mol-1
H2SO4(l)  SO3(g) + H2O(l) △H2 =-130.4 kJ·mol-1
SO3(g) + H2O(l) △H2 =-130.4 kJ·mol-1
2H2SO4(l)  2SO2(g)+ O2(g)+ 2H2O(l) △H3
2SO2(g)+ O2(g)+ 2H2O(l) △H3
则△H3= kJ·mol-1 。
(2)上述热化学循环制氢要消耗大量的能量,从能源角度考虑,可采用的解决方案是
。
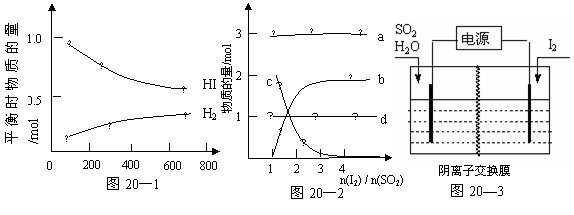
(3)碘化氢热分解反应为:2HI(g) H2(g) + I2(g),分解曲线如图20—1,分解反应平衡常数表达式为:K= ;升高温度时平衡常数K (选填:“增大”或“减小”)。
H2(g) + I2(g),分解曲线如图20—1,分解反应平衡常数表达式为:K= ;升高温度时平衡常数K (选填:“增大”或“减小”)。
(4)本生(Bunsen)反应中SO2和I2及H2O发生的反应为:SO2+I2+2H2O=3H++HSO4-+2I-,
I-+I2 I3-。
I3-。
①当起始时,SO2为1mol,水为16mol,溶液中各离子变化关系如图20—2,图中b变化表示的离子是 ;在水相中进行的本生反应必须使水和碘显著过量,但易
引起副反应将反应器堵塞等。写出浓硫酸与HI发生反应生成硫和碘的化学方程式
。
②野村(Nonura)等人提出利用电解的方法进行本生反应,反应原理如图20—3所示,则阳极的电极反应式为 。
科目:高中化学 来源: 题型:
下列说法正确的是
A.活化分子间所发生的碰撞为有效碰撞
B.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大的主要原因之一是增加了单位体积内活化分子的百分数
D.有气体参与的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子总数,从而使反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
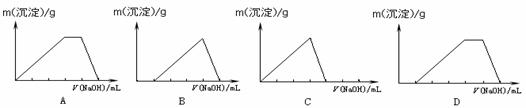
在Al2(SO4)3和(NH4)2SO4的混合溶液中,逐滴加入NaOH溶液至过量。下列图示能正确表示生成沉淀的质量与滴入NaOH溶液体积关系的是( )
查看答案和解析>>
科目:高中化学 来源: 题型:
图示中的四种物质W、X、Y、Z,能按箭头方向一步转化的有
| W | X | Y | Z |
| |
| ① | Na | NaOH | Na2CO3 | NaCl | |
| ② | Al(OH)3 | Al2O3 | Al | NaAlO2 | |
| ③ | SO2 | (NH4)2SO3 | NH4HSO3 | Na2SO3 | |
| ④ | FeCl2 | Fe | FeSO4 | FeCl3 |
A.①②③④ B.①②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
氮氧化物与悬浮在大气中的海盐粒子相互反应:
4NO2(g)+2NaCl(s)  2NaNO3(s)+2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g)
在恒温条件下,向2L恒容密闭容器中加入0.4molNO2和0.2molNaCl,10min反应达到平衡时n(NaNO3)=0.1mol。下列叙述中正确的是
A.10min内NO浓度变化表示的速率v(NO)=0.01 mol·L-1·min-1
B.若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于50%
C.若升高温度,平衡逆向移动,则该反应的△H >0
D.若起始时向容器中充入NO2(g) 0.2mol、NO(g) 0.1mol和Cl2(g) 0.1mol(固体物质足量),则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表。
| 化合物 | 相对分子质量 | 密度/g·cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
(一)乙酸正丁酯的制备
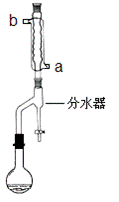
①在干燥的50mL圆底烧瓶中,加入13.5mL正丁醇和7.2mL冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石。然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应
(二)产品的精制
②将分水器分出的酯层和反应液一起倒入分液漏斗中,用10 mL的水洗涤。有机层继续用10 mL10%Na2CO3洗涤至中性,再用10 mL 的水洗涤,最后将有机层转移至锥形瓶中,再用无水硫酸镁干燥。
③将干燥后的乙酸正丁酯滤入50 mL 烧瓶中,常压蒸馏,收集125~127 ℃的馏分,得11.6 g乙酸正丁酯
请回答有关问题。
(1)冷水应该从冷凝管 ___________(填a或b)管口通入。
(2)步骤①中不断从分水器下部分出生成的水的目的是_________________________
步骤①中判断反应终点的依据是_____________________________________。
(3)产品的精制过程步骤②中,第一次水洗的目的是_____________________________,用饱和Na2CO3溶液洗涤有机层,该步操作的目的是_________________________________。
(4)下列关于分液漏斗的使用叙述正确的是____
A.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
B.装液时,分液漏斗中液体的总体积不得超过其容积的2/3
C.萃取振荡操作应如右图所示
D.放出液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
(5)步骤③的常压蒸馏,需收集126℃的馏分,沸点大于140℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管,可能原因是_________________________
(6)该实验过程中,生成乙酸正丁酯(式量116)的产率是__________
查看答案和解析>>
科目:高中化学 来源: 题型:
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:
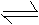 2N2O5(g) 4NO2(g)+O2(g) ΔH>0 ;T1温度下的部分实验数据为:
2N2O5(g) 4NO2(g)+O2(g) ΔH>0 ;T1温度下的部分实验数据为:
| t/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是( )
A.500 s内N2O5分解速率为2.96×10-3 mol·(L·s)-1
B.T1温度下的平衡常数为K1=125, 1000 s时转化率为50%
C.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3
D.其他条件不变时,T2温度下反应到1000 s时测得N2O5(g)浓度为2.98 mol·L-1,则T1<T2
查看答案和解析>>
科目:高中化学 来源: 题型:
利用如图所示的装置,可以验证NH3和HCl的有关性质。实验前a、b、c活塞均关闭。
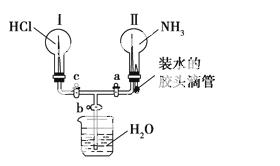
(1)若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是________。
(2)若先打开a、c活塞,再挤压胶头滴管(假设NH3不被完全吸收),在烧瓶Ⅱ中可观察到的现象是___________________________。
(3)通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一同学分析硫元素的化合价有-2、0、+4、+6,而硫单质处于中间价态,所以硫应该既有氧化性,又有还原性。该同学欲探究硫的还原性,下面是该同学的实验探究过程,请解答其中的问题。
(1)该同学应该选择________(填“氧化剂”或“还原剂”)进行实验探究。
(2)该同学用红热的玻璃棒引燃了石棉网上的硫粉,硫粉开始燃烧,反应的化学方程式为_______________________。
(3)该同学欲验证硫燃烧产物的性质,请你帮助他选择合适的试剂,并说明原因。
A.新制的氯水 B.品红溶液
C.滴有酚酞的NaOH稀溶液 D.H2S气体
| 性质 | 试剂 | 化学方程式 |
| 漂白性 | ||
| 氧化性 | ||
| 还原性 | ||
| 酸性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com