
| A. | KClO3+6HCl═3Cl2↑+KCl+3H2O反应中还原剂与氧化剂的物质的量之比为6:1 | |
| B. | 硝酸铵受热分解的化学方程式为:5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O,在反应中被氧化与被还原的氮原子数之比为5:3 | |
| C. | 工业上制备新型净水剂高铁酸钾(K2FeO4)的一步反应如下:2FeCl3+10NaOH+3NaClO═2Na2FeO4+9NaCl+5H2O,若有2 mol FeCl3发生反应,转移电子的物质的量为6 mol | |
| D. | 氮化铝广泛应用于电子陶瓷等工业领域.在一定条件下,AlN可通过反应:Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO合成,方程式中AlN中氮的化合价为-3 |
分析 A.该反应氯酸钾中Cl元素化合价由+5价变为0价、参加反应的$\frac{5}{6}$HCl中Cl元素化合价由-1价变为0价;
B.该反应中铵根离子中N元素化合价由-3价变为0价,硝酸根离子中有$\frac{3}{5}$的N元素化合价由+5价变为0价;
C.该反应中Fe元素化合价由+3价变为+6价,NaClO中Cl元素化合价由+1价变为-1价;
D.AlN中Al元素化合价为+3价.
解答 解:A.该反应氯酸钾中Cl元素化合价由+5价变为0价、参加反应的$\frac{5}{6}$HCl中Cl元素化合价由-1价变为0价,氯酸钾是氧化剂、$\frac{5}{6}$HCl是还原剂,则还原剂和氧化剂的物质的量之比为5:1,故A错误;
B.该反应中铵根离子中N元素化合价由-3价变为0价,硝酸根离子中有$\frac{3}{5}$的N元素化合价由+5价变为0价,铵根离子被氧化、$\frac{3}{5}$的硝酸根离子被还原,则被氧化与被还原的氮原子数之比为5:3,故B正确;
C.该反应中Fe元素化合价由+3价变为+6价,NaClO中Cl元素化合价由+1价变为-1价,若有2 mol FeCl3发生反应,转移电子的物质的量=2mol×(6-3)=6 mol,故C正确;
D.AlN中Al元素化合价为+3价,根据化合物中各元素化合价代数和为0知,N元素化合价为-3价,故D正确;
故选A.
点评 本题考查氧化还原反应,为高频考点,侧重考查学生分析判断及计算能力,明确元素化合价变化及基本概念是解本题关键,注意A中并不是所有的HCl都作还原剂,为易错点.


科目:高中化学 来源: 题型:选择题
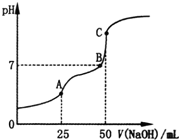
| A. | HC2O4-的电离程度大于其水解程度 | |
| B. | B点时溶液中含有Na2HC2O4和Na2C2O4 | |
| C. | C点时,c(Na+)>c(C2O42-)>c(HC2O4- )>c(OH-)>c(H+) | |
| D. | A点时,c(Na+)+c(H+)═c(OH-)+c(HC2O4-)+2c(C2O42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
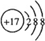 ,
,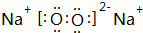 ,用电子式表示C2B的形成过程
,用电子式表示C2B的形成过程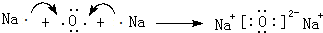
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 工业上用电解MgCl2溶液的方法冶炼Mg | |
| B. | 钢铁发生吸氧腐蚀的正极反应式为4OH--4e-═O2↑+2H2O | |
| C. | 如图中发生反应的方程式为:Fe+2H+=Fe2++H2↑ | |
| D. | 碱性锌锰干电池放电时的正极反应为:MnO2+H2O+e-=MnOOH+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
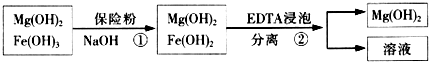
| 精制阻燃剂的条件 | 阻燃剂铁含量 | |||
| 序号 | 提纯体系温度/℃ | 加入EDTA质量/g | 加入保险粉质量/g | W(Fe)/(10-4g) |
| 1 | 40 | 0.05 | 0.05 | 7.63 |
| 2 | 40 | 0.05 | 0.10 | 6.83 |
| 3 | 60 | 0.05 | 0.10 | 6.83 |
| 4 | 60 | 0.10 | 0.10 | 6.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
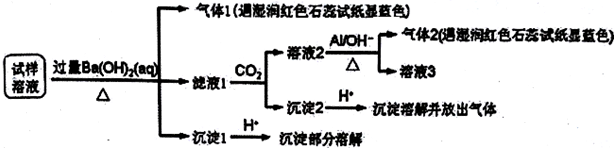
| A. | 试样中肯定存在NH4+、Mg2+、SO42-和NO3- | |
| B. | 该雾霾中可能存在NaNO3、NH4Cl和MgSO4 | |
| C. | 试样中可能存在Na+、Cl- | |
| D. | 试样中一定不含Al3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com