
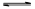 KI3
KI3| A.Na2S2O3 | B.AlCl3 | C.Na2CO3 | D.NaNO2 |
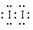 ②5I-+IO3—+6H+=3I2+3H2O、2Fe3++2I―
②5I-+IO3—+6H+=3I2+3H2O、2Fe3++2I― 2Fe2++I2。
2Fe2++I2。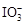 >Fe3+>I2”, 加足量KI后,
>Fe3+>I2”, 加足量KI后,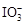 和Fe3+均能将I-氧化成I2,由此也可以知道该加碘盐添加KIO3;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。由此可知该加碘盐中不含KI。所以,①该加碘盐溶液中加KSCN溶液显红色的物质是Fe(SCN)3; CCl4中显紫红色的物质是I2,电子式
和Fe3+均能将I-氧化成I2,由此也可以知道该加碘盐添加KIO3;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。由此可知该加碘盐中不含KI。所以,①该加碘盐溶液中加KSCN溶液显红色的物质是Fe(SCN)3; CCl4中显紫红色的物质是I2,电子式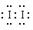 ②第二份试液中加入足量KI固体后,反应的离子方程式为:
②第二份试液中加入足量KI固体后,反应的离子方程式为: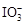 +5I-+6H+
+5I-+6H+ 3I2+3H2O ; 2Fe3++2I―
3I2+3H2O ; 2Fe3++2I― 2Fe2++I2。
2Fe2++I2。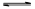 KI3”,可以推出:KI3在常温下不稳定性,受热(或潮湿)条件下易分解为KI和I2 ,KI又易被空气中的氧气氧化,I2易升华,所以KI3·H2O作为食盐加碘剂是不合适的。
KI3”,可以推出:KI3在常温下不稳定性,受热(或潮湿)条件下易分解为KI和I2 ,KI又易被空气中的氧气氧化,I2易升华,所以KI3·H2O作为食盐加碘剂是不合适的。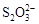 >I-”和氧化还原反应的强弱规律,可以选Na2S2O3作稳定剂;又由题给信息“3I2+6OH-
>I-”和氧化还原反应的强弱规律,可以选Na2S2O3作稳定剂;又由题给信息“3I2+6OH-
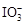 +5I-+3H2O”,可知I2与OH―会发生反应生成
+5I-+3H2O”,可知I2与OH―会发生反应生成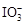 和5I-,而Na2CO3水解呈碱性,因而也可以用Na2CO3作稳定剂,防止加碘盐(添加KI)在潮湿环境下被氧气氧化。至于AlCl3,水解后呈酸性,且还原性I~ > Cl― ,所不能作稳定剂;NaNO2当遇强还原性物质时能表现出氧化性,所NaNO2与KI能发生氧化还原反应:2NO2-+ 2I―+ 4H+=" 2NO↑+" I2+2H2O ,不能作稳定剂。
和5I-,而Na2CO3水解呈碱性,因而也可以用Na2CO3作稳定剂,防止加碘盐(添加KI)在潮湿环境下被氧气氧化。至于AlCl3,水解后呈酸性,且还原性I~ > Cl― ,所不能作稳定剂;NaNO2当遇强还原性物质时能表现出氧化性,所NaNO2与KI能发生氧化还原反应:2NO2-+ 2I―+ 4H+=" 2NO↑+" I2+2H2O ,不能作稳定剂。

科目:高中化学 来源:不详 题型:填空题
| A.酒精灯 | B.长直玻璃导管 | C.锥形瓶 | D.直型冷凝管 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合气体中氯气物质的量为0.04 mol |
| B.混合气体中SO2物质的量为0.04 mol |
| C.所得的沉淀为0.1 mol BaSO4 |
| D.a的取值范围为1.344< a <1.792 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应中氧化剂是Cl2 |
| B.根据该反应可判断还原性:S2O32- > Cl- |
| C.上述反应中,每生成l mol SO42-,转移4 mol电子 |
| D.SO2与氯气的漂白原理相同,所以也可以用SO2做纺织工业的漂白剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化学方程式中按物质顺序的计量数是:8、2、5、1、4、1、5 |
| B.反应中氧化产物是N2O |
| C.反应过程中转移的电子数为8mol电子 |
| D.氧化产物和还原产物的物质的量之比为4∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
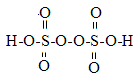
| A.CuO | B.MnO2 | C.Fe2O3 | D.NaNO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.当有0.2 mol CO2生成时,溶液中阴离子的物质的量增加1mol |
| B.该反应中,每有2molCN-反应,转移电子为10mol |
| C.上述反应中的还原剂是OH- |
| D.还原性:Cl-> CN- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.亚硝酸盐有强氧化性 |
| B.普通血红蛋白有较强氧化性 |
| C.亚硝酸盐中毒后,使用美蓝,高铁血红蛋白被还原 |
| D.中毒与解毒过程中都发生了氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com