
| 0.18g |
| 18g/mo |
| 0.224L |
| 22.4L/mol |
| 0.16g |
| 16g/mol |
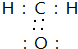 ,故答案为:
,故答案为: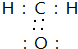 ;
;

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
| A、两种气体中含有相同的质子数 |
| B、SO2与CO2的密度之比为16:11 |
| C、SO2与CO2的质量之比为16:11 |
| D、SO2与CO2含有的电子数之比为16:11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
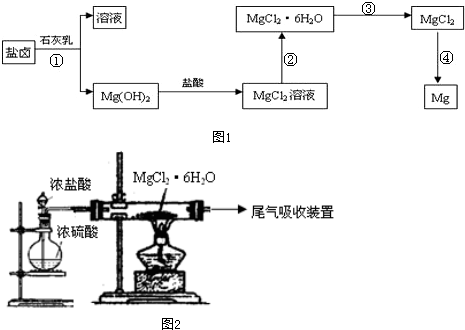
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚乙烯可发生加成反应 |
| B、石油干馏可得到汽油、煤油等 |
| C、淀粉、蛋白质完全水解的产物互为同分异构体 |
| D、从碘水中提取单质碘时,不能用无水乙醇代替CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
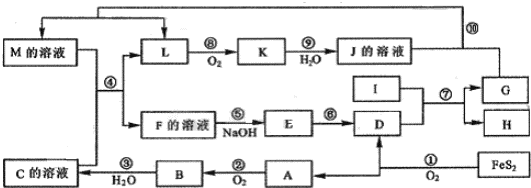
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④①⑤ |
| B、②①③⑤④ |
| C、②①⑤④③ |
| D、②①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com