
【题目】回答实验室配制0.1 mol/L的NaOH溶液500 mL实验中的下列问题。
(1)需NaOH_________g。
(2)有以下仪器:
①烧杯 ②100 mL量筒 ③药匙 ④500 mL容量瓶 ⑤胶头滴管 ⑥托盘天平,配制时,还缺少的玻璃仪器是__________________。
(3)下列称量NaOH的操作中,正确的是_______________。(填序号,下同)
①把NaOH直接放在托盘上称量
②把NaOH放在称量纸上称量
③把NaOH放入烧杯中称量
(4)使用容量瓶前必须进行的一步操作是_____________________________。
(5)配制过程中,下列操作会引起误差偏高的是_______________________。
①未洗涤烧杯、玻璃棒
②NaOH溶液未冷却至室温就转移到容量瓶中
③容量瓶不干燥,含有少量蒸馏水
④称量NaOH的时间太长
⑤定容时俯视刻度
【答案】2 玻璃棒 ③ 检查容量瓶是否漏水 ②⑤
【解析】
根据配制一定物质的量浓度溶液的实验原理、步骤、仪器分析解答,依据![]() 进行误差分析。
进行误差分析。
(1)配制0.1mol/L的NaOH溶液500mL,应选择500ml容量瓶,配制500ml溶液,需要氢氧化钠的质量m=0.1mol/L×0.5L×40g/mol=2.0g;故答案为:2.0;
(2)配制顺序是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒23次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线12cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀。所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,故答案为:玻璃棒;
(3)氢氧化钠具有腐蚀性,应放在小烧杯中称量,故答案为:③;
(4)容量瓶使用之前应先需检查是否漏水,故答案为:检查容量瓶是否漏水;
(5)①未洗涤烧杯、玻璃棒,导致溶质的物质的量偏小,溶液的浓度偏低,故不选;
②NaOH溶液未冷却至室温就转移到容量瓶中,冷却后溶液的体积小于500ml,溶液的浓度偏高,故选;
③容量瓶不干燥,含有少量蒸馏水,对溶质的物质的量和溶液的体积都不会产生影响,溶液浓度不变,故不选;
④称量NaOH的时间太长,氢氧化钠吸收空气中的水和二氧化碳,称取的氢氧化钠的物质的量偏小,溶液的浓度偏低,故不选;
⑤定容时俯视刻度,导致溶液的体积偏小,溶液的浓度偏高,故选;故答案为:②⑤。


科目:高中化学 来源: 题型:
【题目】I.配制![]() 的
的![]() 溶液时,如果只存在下列问题,溶液的浓度如何变化?(填“偏大”“偏小”或“不变”)
溶液时,如果只存在下列问题,溶液的浓度如何变化?(填“偏大”“偏小”或“不变”)
(1)向容量瓶中加蒸馏水低于刻度线,其结果_____________;
(2)定容时观察刻度线仰视,其结果_____________。
II.(1)实验室加热固体氯化铵和氢氧化钙的混合物制取氨,反应的化学方程式为:__________________________。
(2)请在下列装置中选择实验室制备氨的发生装置:_____________(将编号字母填入空格处,下同);为了得到纯净的氨,请在下列试剂中选择干燥氨的试剂:_____________。
装置有:
A B
B![]() C
C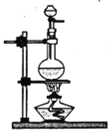 D
D![]() E
E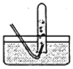 F
F![]() G
G![]() H
H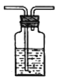
试剂有:a.![]() 溶液b.澄清石灰水c.浓硫酸d.饱和
溶液b.澄清石灰水c.浓硫酸d.饱和![]() 溶液e.碱石灰f.品红溶液g.湿润的红色石蕊试纸
溶液e.碱石灰f.品红溶液g.湿润的红色石蕊试纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用有关概念,判断下列叙述正确的是![]()
A.![]() 溶于水后能导电,故C
溶于水后能导电,故C![]() 为电解质
为电解质
B.![]() 、
、![]() 、
、![]() 、
、![]() 互为同素异形体
互为同素异形体
C.NaCl溶液和![]() 溶液均显中性,故两溶液中水的电离程度相同
溶液均显中性,故两溶液中水的电离程度相同
D.溶液与胶体本质区别为分散质微粒直径的大小不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铁质容器盛装冷浓硫酸。某学习小组进行了以下探究活动:
(探究一)
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是___________________。
(2)另取该铁钉样品放入一定体积的浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。取336 mL(标准状况)气体Y通入足量溴水中,发生反应的离子方程式为__________________,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33 g。由此推知气体Y中SO2的体积分数为___________。
(探究二)
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
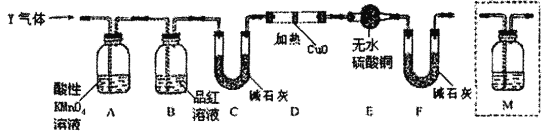
(3)装置B的作用是___________________。
(4)认为气体Y中还含有Q的理由是________________________________(用化学方程式表示)。
(5)为确认Q的存在,则M中盛放的试剂为___________,需将装置M添加于________(填序号)。
a.A之前 b.A—B间 c.B—C间 d.C—D间
(6)如果气体Y中含有H2,预计实验现象应是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应是氧化还原反应的是( )
A.AgNO3 + HCl ==AgCl↓+ HNO3
B.NH4HCO3 ![]() NH3↑+ CO2↑+ H2O
NH3↑+ CO2↑+ H2O
C.2KClO3 ![]() 2KCl+3O2↑
2KCl+3O2↑
D.CaO+H2O ==Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为短周期元素。A、B可形成两种液态化合物甲和乙,其最简式分别为BA和B2A。A与D可形成气态化合物DA、DA2。A、B、D可组成离子化合物,该晶体化学式为B4A3D2,其水溶液呈弱酸性。B与D可形成一种极易溶于水的碱性气体X。B与C可形成极易溶于水的酸性气体Y。已知X分子与乙分子中的电子数相等,Y分子与甲分子中的电子数相等。请回答:
(1)A元素为___,甲的电子式为____________。
(2)常温下,pH为a的Y溶液与pH为b的氢氧化钠溶液按体积比1∶10混合后,正好完全反应,则a与b的关系为______。
(3)已知X在液态时和水一样,可发生微弱的电离,产生两种含相同电子数的粒子,请写出它电离方程式:____________________。
(4)将X和Y的稀溶液按某种比例混合,
①若所得溶液中只含一种溶质,则该溶质是______,溶液中离子浓度的大小顺序为____________________________;
②若该溶液是由体积相等的X和Y溶液混合而成,且恰好呈中性,则混合前c(X)____c(Y),混合前酸中c(H+)和碱中c(OH-)的关系c(H+)____c(OH-)(填“大于”、“等于”、“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,CH3COOH的电离平衡常数为1.7×10-5。
(1)CH3COOH的电离方程式为_________。25℃,0.1mol/LCH3COOH溶液中计算c(H+)的表达式为__________。
(2)25℃时,CH3COONa稀溶液中的水解平衡常数等于_____ (保留小数点后一位数字)。
(3)25℃,0.1 mol/LCH3COONa溶液的pH最接近______(填选项)。
A.9 B.10 C.11 D.12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。(已知:Na2SO3+ H2SO4(浓)=Na2SO4+SO2↑+H2O)
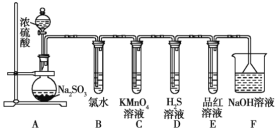
请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠仪器的名称分别是______、______。
(2)反应后,装置B中产生的现象是______,发生反应的离子方程式为______;装置D中的现象是______,发生反应的化学方程式为______。
(3)装置E的目的是探究SO2与品红溶液作用的可逆性,写出实验操作及现象:____________。
(4)F装置的作用是______,倒扣漏斗的作用是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2014年3月22日是第二十二届“世界水日”,保护水资,从我做起!
(1)ClO2和Cl2(还原产物都为Cl-)是生活中常用的消毒剂。当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的_______倍。
(2)炼金废水中含有络离子[Au(CN)2]+,与弱电解质碳酸的电离方式相似,[Au(CN)2]+也存在着两步电离,其电离出CN-有毒,CN-与H+结合生成毒性更强的HCN。[Au(CN)2]+的一级电离方程式:__________________________;在碱性条件下NaClO将废水中的CN-氧化成CO![]() 和N2,其反应的离子方程式为: _______________________________________________ 。
和N2,其反应的离子方程式为: _______________________________________________ 。
(3)某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-离子中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关现象如下图所示:

请根据上图回答下列问题:
①实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为________________。
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为_______________________________。
③试确定NO3-是否存在?_________________(填“存在”、“不存在”或“不确定”),若存在,试计算c(NO3-)_________________(若不存在,此问不必作答)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com