

 ��ԭ�ͣ���ɫ��
��ԭ�ͣ���ɫ��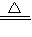 CuSO4+SO2+2H2O����ƽ���ƶ��ĽǶȼ���ƽ��ʱ�����ʵ�Ũ�ȣ��������㻯ѧƽ�ⳣ���Լ��жϸ����ʵ�Ũ�ȵı仯��
CuSO4+SO2+2H2O����ƽ���ƶ��ĽǶȼ���ƽ��ʱ�����ʵ�Ũ�ȣ��������㻯ѧƽ�ⳣ���Լ��жϸ����ʵ�Ũ�ȵı仯��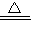 CuSO4+SO2+2H2O��
CuSO4+SO2+2H2O��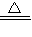 CuSO4+SO2+2H2O��
CuSO4+SO2+2H2O��  2SO3
2SO3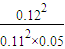 =23.8
=23.8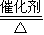 2SO3
2SO3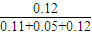 =0.429��
=0.429�� =
=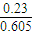 =0.380��
=0.380��

 �����Ļ���������人������ϵ�д�
�����Ļ���������人������ϵ�д� ���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д�
���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д� ��ٽ������½������������ϵ�д�
��ٽ������½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ||
| ||
 ��ԭ�ͣ���ɫ��
��ԭ�ͣ���ɫ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�Իش���������:
(1)M�ĵ���ʽΪ:_______________��M��������������֮��Ϊ:_______________��
(2)G�ڷ�Ӧ�٣����зֱ���_______________����_______________����
(3)д�����з�Ӧ�Ļ�ѧ����ʽ:
A+B��C+D:______________________________��
D+M��L:________________________________��
F��G�������B��E:______________________________��
(4)д�����з�Ӧ�����ӷ���ʽ:
K+E+D��I+H:______________________________��
I+G��K+E+J:______________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com