
| A£® | Ķ¼ČæÉŅŌ·¢ÉśĪöĒāøÆŹ“Ņ²æÉŅŌ·¢ÉśĪüŃõøÆŹ“ | |
| B£® | ĢśÖ»ÄÜ·¢ÉśĪöĒāøÆŹ“ | |
| C£® | ĶÖ»ÄÜ·¢ÉśĪüŃõøÆŹ“ | |
| D£® | ĪöĒāøÆŹ“±ČĪüŃõøÆŹ“ĘÕ±é |
·ÖĪö Ķ»īĘĆŠŌ±ČĒāČõ£¬¶ųĢś±ČĒāĒ棬ĖłŅŌĶ²»ÄÜ·¢ÉśĪöĒāøÆŹ“Ö»ÄÜ·¢ÉśĪüŃõøÆŹ“£¬Ģś¼ČæÉŅŌ·¢ÉśĪöĒāøÆŹ“Ņ²æÉŅŌ·¢ÉśĪüŃõøÆŹ“£¬¾Ż“Ė·ÖĪö£®
½ā“š ½ā£ŗA£®Ķ»īĘĆŠŌ±ČĒāČõ£¬²»ÄÜ·¢ÉśĪöĒāøÆŹ“£¬¹ŹA“ķĪó£»
B£®Ģś»īĘĆŠŌ±ČĒāĒ棬ĖłŅŌĢś¼ČæÉŅŌ·¢ÉśĪöĒāøÆŹ“Ņ²æÉŅŌ·¢ÉśĪüŃõøÆŹ“£¬¹ŹB“ķĪó£»
C£®Ķ»īĘĆŠŌ±ČĒāČõ£¬²»ÄÜ·¢ÉśĪöĒāøÆŹ“£¬Ö»ÄÜ·¢ÉśĪüŃõøÆŹ“£¬¹ŹCÕżČ·£»
D£®ĪüŃõøÆŹ“±ČĪöĒāøÆŹ“Ęձ飬¹ŹD“ķĪó£»
¹ŹŃ”£ŗC£®
µćĘĄ ±¾Ģāæ¼²éĮĖ½šŹōµÄøÆŹ“Óė·Ą»¤£¬×¢ŅāĶ»īĘĆŠŌ±ČĒāČõ£¬²»ÄÜ·¢ÉśĪöĒāøÆŹ“£¬ĢāÄæÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 ŹµŃéŹŅŠčŅŖ0.80mol•L-1 NaOHČÜŅŗ475mLŗĶ0.40mol•L-1ĮņĖį500mL£®øł¾ŻÕāĮ½ÖÖČÜŅŗµÄÅäÖĘĒéæö»Ų“šĻĀĮŠĪŹĢā£ŗ
ŹµŃéŹŅŠčŅŖ0.80mol•L-1 NaOHČÜŅŗ475mLŗĶ0.40mol•L-1ĮņĖį500mL£®øł¾ŻÕāĮ½ÖÖČÜŅŗµÄÅäÖĘĒéæö»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØClO-£©=1.0mol/LµÄČÜŅŗÖŠ£ŗNa+”¢SO32-”¢S2-”¢SO42- | |
| B£® | ³£ĪĀĻĀ£¬$\frac{c£Ø{H}^{+}£©}{c£ØO{H}^{-}£©}$=10-10µÄČÜŅŗÖŠ£ŗCa2+”¢Mg2+”¢HCO3-”¢I- | |
| C£® | µĪČėÉŁĮæKSCNČÜŅŗĻŌŗģÉ«µÄČÜŅŗÖŠ£ŗNa+”¢K+”¢I-”¢SO42- | |
| D£® | ÓÉĖ®µēĄėµÄc£ØH+£©=1”Į10-12mol/LµÄČÜŅŗÖŠ£ŗBa2+”¢K+”¢Cl-”¢NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
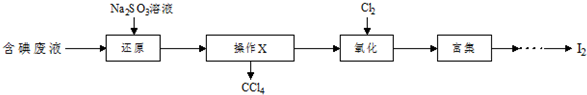
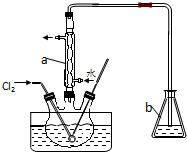
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČŻĮæĘæ²»æÉŅŌÓĆĄ“Čܽā¹ĢĢ壬µ«æÉŅŌÓĆĄ“Ļ”ŹĶÅصÄČÜŅŗ | |
| B£® | “ÖŃĪĢį“æŹ±¹żĀĖĖłÓĆĘÕĶØĀ©¶·ÓėŻĶČ”ĖłÓĆ·ÖŅŗĀ©¶·½į¹¹ŹĒŅ»ŃłµÄ | |
| C£® | ÓĆ50mLĮæĶ²æÉ×¼Č·ÅäÖĘ50mL0.10mol/LµÄĢ¼ĖįÄĘČÜŅŗ | |
| D£® | ŹµŃéŹŅÖĘÕōĮóĖ®Ź±ĄäÄż¹ÜŅŖ”°ĻĀ½ųĖ®”¢ÉĻ³öĖ®”±²¢±£»¹Ė®µÄ³ÖŠųĮ÷¶Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C2H5OH | B£® | C6H5OH | C£® | H2O | D£® | CH3COOH |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com