
| ||
| 200--250�� |
| ||
| 200--250�� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶ȣ�K�� | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1 173 | 2.15 | 1.67 |
| A����Ӧ���Ƿ��ȷ�Ӧ |
| B����Ӧ���Ƿ��ȷ�Ӧ |
| C����Ӧ����973Kʱ����ѹǿ��K2���� |
| D���ڳ����·�Ӧ��һ�����Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| c HCN-c CN- |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� | ||
| 4 | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
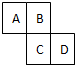 ��ͼΪԪ�����ڱ���һ���֣���֪A��B��C��D��Ϊ������Ԫ�أ�A��Dԭ������֮����C��ԭ��������1.5����
��ͼΪԪ�����ڱ���һ���֣���֪A��B��C��D��Ϊ������Ԫ�أ�A��Dԭ������֮����C��ԭ��������1.5�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 | |
| ��2���� | �� | �� | ||||||
| ��3���� | �� | �� | �� | �� | �� | �� | ||
| ��4���� | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �ŵ� |
| ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����A��ʾ�ķ�Ӧ������0.4mol/��L?min�� |
| B����C��ʾ��������0.2mol/��L?min�� |
| C����2minĩ�ķ�Ӧ���ʣ���B��ʾ��0.3mol/��L?min�� |
| D����D��ʾ�ķ�Ӧ������0.2mol/��L?min�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com