

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���

| ���� | ��ʼ���� | ������ȫ |
| Fe��OH��3 | 2.7 | 3.7 |
| Fe��OH��2 | 7.6 | 9.6 |
| Mn��OH��2 | 8.3 | 9.8 |
| Mg��OH��2 | 9.6 | 11.1 |
| �Լ� | �۸�Ԫ/�֣� |
| ƯҺ����NaClO��25.2%�� | 450 |
| ˫��ˮ����H2O2��30%�� | 2400 |
| �ռ��98%NaOH�� | 2100 |
| �����99.5%Na2CO3�� | 600 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
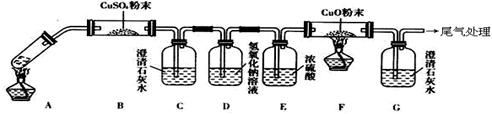
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��װ�â��ܿ��Ʒ�Ӧ�ķ����ͽ��� |
| B��������Ӧ��ڵ��Թ�ȡ�£���ͨ����м��ȣ�������̼�����ζ�����壬��Һ�ʺ�ɫ |
| C������ʯ����Һ���ɫ |
| D��Ϊȷ��CuSO4���ɣ�����м�ˮ���۲���Һ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
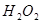 �ֽⷴӦ���ʵ�Ӱ�죬ijͬѧ����֧�Թ��зֱ����
�ֽⷴӦ���ʵ�Ӱ�죬ijͬѧ����֧�Թ��зֱ����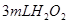 ��Һ���������ռ�
��Һ���������ռ�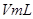 ���������ʱ�䣬ʵ���¼���£�
���������ʱ�䣬ʵ���¼���£�| ʵ����� | 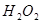 ��ҺŨ�� ��ҺŨ�� | 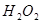 ��Һ�¶� ��Һ�¶� | ���� | ����ʱ�� |
| �� | 5% | 20�� | 2��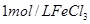 | 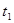 |
| �� | 5% | 40�� | 2��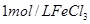 | 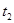 |
| �� | 10% | 20�� | 2��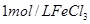 | 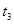 |
| �� | 5% | 20�� | ��ʹ�� | 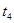 |
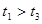 ��ԭ����__________��
��ԭ����__________��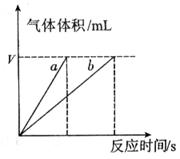
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| ʵ�� ��� | ���/mL | ||||
| K2S2O8��Һ | ˮ | KI��Һ | Na2S2O3��Һ | ������Һ | |
| �� | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| �� | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| �� | 8.0 | VX | 4.0 | 4.0 | 2.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����


�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com