
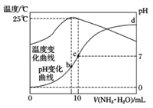
【题目】在某温度时将 ![]() 氨水滴入
氨水滴入 ![]() 盐酸中,溶液 pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
盐酸中,溶液 pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
A.![]()
B.水的电离程度:![]()
C.c点:![]()
D.d点:![]()
【答案】D
【解析】
A.如果a=1,当体积为10ml时两者恰好完全反应生成氯化铵,是强酸弱碱盐水解呈酸性,所以a>1,故A错误;
B.b点溶液温度最高,说明此时两溶液恰好反应生成氯化铵,NH4+水解促进了水的电离,c点溶液呈中性,则溶质为NH4Cl和NH3H2O,NH3H2O抑制了NH4+的水解,则b点溶液中水的电离程度大于c点溶液中水的电离程度,故B错误;
C.c点溶液呈中性,所以c(H+)=c(OH-),由电荷守恒分析c(NH4+)+c(H+)=c(Cl-)+c(OH-),所以c(NH4+)=c(Cl-)=0.05mol/L,故C错误;
D.d点溶液呈碱性,氨水过量,溶液中为NH4Cl和氨水,溶液中存在电荷守恒:c(NH4+)+c(H+)=c(OH-)+c(Cl-),由于c(H+)<c(OH-),所以c(Cl-)<c(NH4+),故D正确;
故答案为D。


科目:高中化学 来源: 题型:
【题目】(Ⅰ)CoCl2溶液能发生如下变化:
CoCl2![]() Co(OH)2
Co(OH)2![]() [Co(NH3)6]2+
[Co(NH3)6]2+![]() X
X![]() 晶体Y(CoCl3·5NH3)
晶体Y(CoCl3·5NH3)
向X溶液中加入强碱并加热至沸腾有氨气放出,同时产生Co2O3沉淀;若向Y的溶液中加AgNO3溶液,有AgCl沉淀生成,滤出沉淀,再向滤液中加入AgNO3溶液无变化,但加热至沸腾时又有AgCl沉淀生成,其沉淀量为上次沉淀量的一半。请回答下列问题:
(1)反应②的离子方程式是__________________________________________。
(2)反应①~③中属于氧化还原反应的是______,配合物Y的化学式为______。
(Ⅱ)一定条件下,将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,发生反应CH4(g)+H2O(g) ![]() CO(g)+3H2(g),达到平衡时测得CO的物质的量为0.10mol。若平衡常数K=27,试计算(要求写出计算过程,计算结果保留两位有效数字):
CO(g)+3H2(g),达到平衡时测得CO的物质的量为0.10mol。若平衡常数K=27,试计算(要求写出计算过程,计算结果保留两位有效数字):
(1)初始加入容器的甲烷的物质的量__________;
(2)平衡时CH4的体积分数__________;
(3)若温度不变时再向上述平衡混合物中加入0.01molH2O(g)和0.1molCO,平衡是否移动__________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向![]() 溶液中逐滴加入
溶液中逐滴加入![]() 盐酸,溶液含R微粒的物质的量分数与pH关系如图所示
盐酸,溶液含R微粒的物质的量分数与pH关系如图所示![]() 不稳定,易转化为
不稳定,易转化为![]() 气体逸出溶液,气体逸出未画出,忽略因气体逸出引起的溶液体积变化
气体逸出溶液,气体逸出未画出,忽略因气体逸出引起的溶液体积变化![]() 下列说法错误的是
下列说法错误的是![]()

A.![]() 溶液中:
溶液中:![]()
B.当溶液![]() 时,溶液总体积大于40mL
时,溶液总体积大于40mL
C.在B点对应的溶液中,离子浓度最大的是![]()
D.A点对应pH约为![]() ,
,![]() 的水解常数
的水解常数![]() 数量级为
数量级为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解装置如图所示:

Ⅰ.当用惰性电极电解时,c为____________极, d极的电极反应_________,电解总反应的化学方程____________________
Ⅱ.(1)若用此装置进行铁上镀铜则c为__________(填铁或铜),电解液浓度_____________(增大,减小或不变)
(2)电镀一段时间后对电极进行称量发现两极质量差为16克,则电路中转移的电子___________mol.
Ⅲ.若用此装置进行粗铜的电解精炼。则要求粗铜板是图中电极________(填图中的字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在一定体积的密闭容器中,下列叙述不能作为可逆反应A(g)+3B(g) ![]() 2C(g)达到平衡状态标志的是 ( )
2C(g)达到平衡状态标志的是 ( )
①C的生成速率与C的消耗速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④C的物质的量不再变化
⑤混合气体的总压强不再变化
⑥混合气体的总物质的量不再变化
⑦单位时间消耗a mol A,同时生成3a mol B
⑧A、B、C的分子数之比为1∶3∶2
A. ②⑧B. ④⑦C. ①③D. ⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A. 1mol甲基含10NA个电子
B. 15 g C2H6中含有共价键数目为3NA
C. 标准状况下,11.2 L三氯甲烷所含的分子数目为0.5NA
D. 一定条件下,2.6 g苯和苯乙烯的混合物完全燃烧消耗O2的分子数为0.25NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如下:

下列说法中正确的是( )
A. 反应1→2中原子利用率为90%
B. 检验制得的香草醛中是否混有化合物3,可用氯化铁溶液
C. 化合物2在一定条件下可发生酯化反应
D. 等物质的量的四种化合物分别与足量NaOH溶液反应,消耗NaOH物质的量之比为1∶4∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色;J分子内有两个互为对位的取代基.在一定条件下有如下的转化关系:(无机物略去)
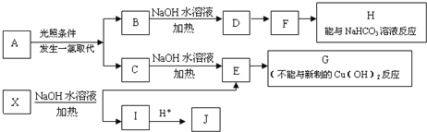
(1)属于芳香烃类的A的同分异构体中,其沸点的大小关系为______;(不包括A,用结构简式表示)
(2)J中所含的含氧官能团的名称为______;
(3)E与H反应的化学方程式是________;反应类型是_______;
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物I,以I为单体合成的高分子化合物的名称是______;
(5)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式_______;
①与FeCl3溶液作用显紫色
②与新制Cu(OH)2悬浊液作用产生红色沉淀
③苯环上的一卤代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%,二氧化碳(CO2)的排放量也要大幅减少。
(1)在恒温,容积为1L恒容容器中,硫可以发生如下转化,其反应过程和能量关系如图1所示(已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6kJmol-1),请回答下列问题:
2SO3(g) ΔH=-196.6kJmol-1),请回答下列问题:
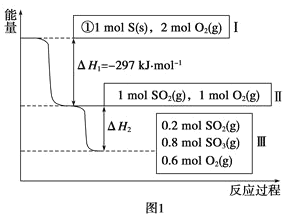
写出能表示硫的燃烧热的热化学方程式:___。
②ΔH2=___kJmol-1。
③在相同条件下,充入1molSO3和0.5mol的O2,则达到平衡时SO3的转化率为___;此时该反应___(填“放出”或“吸收”)___kJ的能量。
(2)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。
①CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0kJmol-1,测得CO2和CH3OH(g)浓度随时间变化如图2所示。从3min到9min,v(H2)=___molL-1min-1。
CH3OH(g)+H2O(g) ΔH=-49.0kJmol-1,测得CO2和CH3OH(g)浓度随时间变化如图2所示。从3min到9min,v(H2)=___molL-1min-1。
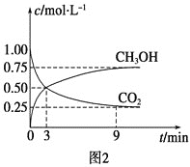
②能说明上述反应达到平衡状态的是___(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1:1
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3molH2,同时生成1molH2O
D.CO2的体积分数在混合气体中保持不变
③为加快化学反应速率且使体系中气体的物质的量减少,其他条件不变时,可采取的措施有___(填编号)。
A.升高温度 B.缩小容器体积 C.再充入水蒸气 D.使用合适的催化剂
(3)工业上,CH3OH也可由CO和H2合成。参考下表中合成反应CO(g)+2H2(g)![]() CH3OH(g)的平衡常数。下列说法正确的是___。
CH3OH(g)的平衡常数。下列说法正确的是___。
温度/℃ | 0 | 100 | 200 | 300 | 400 |
平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
A.该反应正反是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应ΔS<0
C.在T℃时,1L密闭容器中,投入0.1molCO和0.2molH2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5MPa)和250℃,是因为此条件下,原料气转化率最高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com