
下列叙述中正确的是
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B.除短周期外,其它周期均有18种元素
C.在同一周期中,ⅠA族比ⅡA族的单质与水反应更剧烈
D.在ⅠA族中,单质的熔、沸点随着原子半径的增大而逐渐升高
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
航天飞机用高氯酸铵(NH4ClO4)与铝粉的混合物做固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其反应的热化学方程式为:
2NH4ClO4(s)  N2(g)+4H2O(g)+Cl2(g)+2O2(g) H=Q kJ/mol
N2(g)+4H2O(g)+Cl2(g)+2O2(g) H=Q kJ/mol
下列有关上述反应的叙述中,不正确的是
A.属于分解反应
B.瞬间产生大量高温气体推动航天飞机飞行
C.能量变化主要是化学能转化为热能和动能
D.反应中高氯酸铵只起氧化剂作用
查看答案和解析>>
科目:高中化学 来源: 题型:
请根据反应 Fe + CuSO4 = Fe SO4 + Cu,设计原电池,完成以下问题。
负极: ,其电极反应式为:
正极|: ,其电极反应式为:________________________
电解质溶液: __________,电池的总离子反应式为:_
查看答案和解析>>
科目:高中化学 来源: 题型:
降低太气中CO2含量及有效开发利用CO2,是科学家研究的重要课题。
(1)将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g)+6H2(g)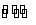 CH3OCH3(g)+3H2O(g) ΔH=122.4kJ·mol-1
CH3OCH3(g)+3H2O(g) ΔH=122.4kJ·mol-1
①某温度下,将2.0molCO2(g)和6.0molH2(g)充入体积可变的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中.CH3OCH3(g)的物质的量分数变化如下表所示。
| P1 | P2 | P3 | |
| T1 | 0.10 | 0.04 | 0.02 |
| T2 | 0.20 | 0.16 | 0.05 |
| T3 | 0.40 | 0.35 | 0.20 |
则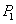 ______
______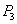 (填“>”“<”或“=”,下同)。若
(填“>”“<”或“=”,下同)。若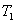 、
、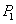 ,
,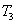 、
、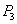 时平衡常数分别为
时平衡常数分别为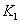 、
、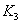 ,则K1_______K3。
,则K1_______K3。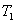 、
、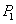 时H2的平衡转化率为________。
时H2的平衡转化率为________。
②一定条件下,上述反应在密闭容器中达平衡。当仅改变影响反应的一个条件,引起的下列变化能说明平衡一定向正反应方向移动的是________。
a.反应物的浓度降低
b.容器内压强增大
c.正反应速率大于逆反应速率
d.化学平衡常数K增大
(2)碳酸氢钾溶液加水稀释,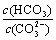 ________(填“增大”“不变”或“减小”)。用碳酸钾溶液吸收空气中CO2,当溶液呈中性时,下列关系或说法正确的是:_______。
________(填“增大”“不变”或“减小”)。用碳酸钾溶液吸收空气中CO2,当溶液呈中性时,下列关系或说法正确的是:_______。
a.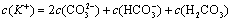
b.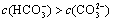
c.降低温度,c(H+)·c(OH-)不变
(3)向盛有FeCl3溶液的试管中滴加少量碳酸钾溶液,立即产生气体,溶液颜色加深,用激光笔照射能产生丁达尔效应,反应的离子方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组元素的原子随着原子序数的递增,有关递变不正确的是
A. 最高正价:P<S<Cl<Ar B. 金属性:Na<K<Rb<Cs
C. 原子半径:C>N>O>F D. 最外层电子数:Na<Mg<Al<Si
查看答案和解析>>
科目:高中化学 来源: 题型:
根据表中信息,判断以下叙述正确的是
部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.氢化物的稳定性为H2T<H2R B.单质与稀盐酸反应的剧烈程度为L<Q
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
今有A、B两种原子,A原子的M层比B原子的M层少2个电子,B原子的L层电子数为A原子L层电子数的2倍。A和B分别是
A.C和Mg B.Si和Na C.Cl和C D. B和He
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合溶液中含有NaI、NaBr、Na2SO4三种溶质,其物质的量均为l mol,向混合溶液中通入一定量的氯气。下列说法正确的是
A.将溶液蒸干最多可以得到4 mol NaCl
B.将溶液蒸干并灼烧,得到的固体可能是NaCl、NaBr、Na2SO4
C.向溶液中滴加KI淀粉溶液,溶液变蓝,则氯气一定过量
D.若通入氯气的体积为11.2 L(标准状况),反应的离子方程式为:2I-+Cl2=I2+2C1-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com