
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源:2013-2014学年上海市杨浦区高三上学期期中考试化学试卷(解析版) 题型:选择题
已知醋酸、醋酸根离子在溶液中存在下列平衡:
CH3COOH+H2O 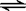 CH3COO—+H3O+
K1=1.75×10-5
CH3COO—+H3O+
K1=1.75×10-5
CH3COO—+H2O 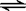 CH3COOH+OH—
K2=5.71×10-10
CH3COOH+OH—
K2=5.71×10-10
现有50 mL 0.2 mol·L-1醋酸与50 mL 0.2 mol·L-1醋酸钠混合制得溶液甲,下列叙述正确的是
A.甲溶液的pH >7
B.对甲进行微热,K1、K2同时增大
C.若在甲中加入很少量的NaOH溶液,溶液的pH几乎不变
D.若在甲中加入5 mL 0.1 mol·L-1的盐酸,则溶液中醋酸的K1会变大
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)现有NaOH和NaHC03固体混合物0.2 mol,在密闭容器中加热到250℃,使其充分反应后,排出气体,冷却,称得残留固体质量为W g.
(1)写出可能发生反应的化学方程式.
(2)设混合物中NaOH为x mol(0<x<0.2).当x取不同值时,推断残留物质的种类,并计算W的数值(可以用含有“x”的代数式表示).请填表回答:
_ X值 |
残留固体(化学式) |
W值(g) |
X=0.1 |
|
|
0<x<0.1 |
|
|
0.1<x<O.2 |
|
|
(3)在下面坐标中,画出w值随x值变化的曲线.

查看答案和解析>>
科目:高中化学 来源: 题型:
工业甲醇的质量分数可以用下列方法测定:
①在稀H2SO4中甲醇被Cr2O72-氧化成CO2和H2O,反应式为:
CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O;
②过量的Cr2O72-可用Fe2+与之完全反应:
_____Cr2O72-+_____Fe2++_____H+ ——_____Cr3++______Fe3++______H2O
现有0.12 g工业甲醇,在H2SO4溶液中与25 mL 0.2 mol·L-1K2Cr2O7溶液反应,多余的K2Cr2O7再用1 mol·L-1FeSO4与其反应,结果用去FeSO4溶液9.6 mL。
(1)配平第②步中离子方程式。
(2)计算工业甲醇的质量分数。(保留小数点后一位有效数字)
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:单选题
[ ]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com