
| A. | 该有机物分子中碳、氢、氧原子个数比为1:2:3 | |
| B. | 该有机物分子中碳、氢原子个数比为1:2 | |
| C. | 该有机物中必含氧元素 | |
| D. | 该有机物中可能不含氧元素 |
分析 因生成CO2和H2O的物质的量比为1:1,则n(C):n(H)=1:(1×2)=1:2,题干信息无法判断有机物分子中是否含有氧元素,以此解答该题.
解答 解:A.只根据生成产物为二氧化碳和水,无法判断该有机物中是否含有氧原子,故A错误;
B.生成CO2和H2O的物质的量比为1:1,则n(C):n(H)=1:(1×2)=1:2,故B正确;
C.该有机物充分燃烧生成二氧化碳和水,其分子中可能含有氧原子,故C错误;
D.题干信息无法确定该有机物分子中是否含有氧原子,故D正确;
故选BD.
点评 本题考查了有机物结构与性质、有机物分子式的确定,题目难度不大,注意明确常见有机物组成、结构与性质,明确确定有机物分子式的方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验现象 |
| (A) |
| (B)反应不十分强烈,产生的气体可在空气中燃烧 |
| (C)剧烈反应,产生可燃性气体 |
| (D)生成白色胶状沉淀,然后沉淀消失 |
| (E)产生气体,可在空气中燃烧,溶液变成浅红色 |
| 实验方案 |
| 1.用砂纸打磨后的镁带加适量水加热,再向反应后溶液中滴加酚酞 |
| 2.钠与滴有酚酞的试液的冷水反应 |
| 3.镁带与2mol/L的盐酸反应 |
| 4.铝条与2mol/L的盐酸反应 |
| 5.向氯化铝溶液中滴加氢氧化钠溶液至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
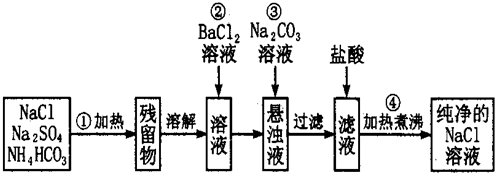
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2240mL | B. | 1008mL | C. | 3360mL | D. | 448mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com