
����Ŀ����1��������ȣ����������к�ǿ�Ŀ���ʴ�ԣ�ԭ����____���Ȼ������Ȼᷢ������������˵���Ȼ�����______��ѡ���������������������������
��2��һ�������£����ݻ�һ���������У�����CO2������Ӧ��Fe(s)+CO2(g) ![]() FeO(s)+CO(g)���÷�Ӧ��ƽ�ⳣ������ʽK=_____________�����д�ʩ����ʹƽ��ʱc(CO)/c(CO2)�������________(ѡ����)
FeO(s)+CO(g)���÷�Ӧ��ƽ�ⳣ������ʽK=_____________�����д�ʩ����ʹƽ��ʱc(CO)/c(CO2)�������________(ѡ����)
a.�����¶� b.����ѹǿ c.����һ����CO d.�ټ���һЩ����
��3��FeS2����Fe2(SO4)3��Һ�����ܽ�������Ԫ�ض���SO42-��ʽ���ڣ�����ɸ÷�Ӧ�Ļ�ѧ����ʽ��
______________________________________________________________________
��4����Һ������Զ��������ʵ��������кܴ�Ӱ��;��������ܽ��Ի�Ӱ�츴�ֽⷴӦ�ķ���Na2S��Һ�μӵ�FeCl3��Һ�У��е���������;��FeCl3��Һ�μӵ�Na2S��Һ�����ɵ���Fe2S3������S��Fe(OH)3�����Ϸ�Ӧ�ɵó��Ľ�����________________________________��
���𰸡� ���ᷢ���绯ѧ��ʴ ���� c(CO)/c(CO2) a FeS2+7Fe2(SO4)3+8H2O��15FeSO4+8H2SO4 ��������������:Fe3+>S������Fe3+������:Fe(OH)3>Fe2S3
����������1��������ȣ����������к�̼���ܵͣ��ڳ�ʪ�Ļ����в������γ�ԭ��أ����Բ��ᷢ���绯ѧ��ʴ������ʴ��ǿ���Ȼ������Ȼᷢ����������˵���Ȼ����е�ͣ�Ϊ���Ӿ��壬�Ȼ����д��ڷ��ӣ�˵���Ȼ�������ԭ������ԭ��ͨ�����ۼ��γɵĹ��ۻ����
��2������ƽ�ⳣ�����ƽ�ⳣ������ʽΪ��������ƽ��Ũ�ȵĻ�ѧ���������ݵij˻������Ӧ��ƽ��Ũ�ȵĻ�ѧ���������ݵij˻��ı�ֵ����Ϊ����ʹ�Һ�岻д�����ʽ�У����Է�ӦFe(s)+CO2(g) ![]() FeO(s)+CO(g)��ƽ�ⳣ������ʽK=
FeO(s)+CO(g)��ƽ�ⳣ������ʽK=![]() ��ƽ�ⳣ�����¶ȱ仯������Ũ��ѹǿ�����ر仯������ʹƽ��ʱ
��ƽ�ⳣ�����¶ȱ仯������Ũ��ѹǿ�����ر仯������ʹƽ��ʱ![]() ����Ĵ�ʩ��a��
����Ĵ�ʩ��a��
��3��FeS2����Fe2(SO4)3��Һ�С��ܽ⡱����Ԫ�ض���SO42-����ʽ���ڣ���Fe3+����S22-����SO42-����������ԭΪFe2+�����ݵ�ʧ�����غ㣬��1molFeS2���ܽ⡱����ҪFe2(SO4)3�����ʵ���= =7mol������Feԭ���غ㣬����FeSO4�����ʵ���=1mol+7mol��2=15mol������Sԭ���غ㣬����H2SO4�����ʵ���=1mol��2+7mol��3-15mol=8mol��������ԭ���غ㣬��8molH2O�μӷ�Ӧ�����Ը÷�Ӧ�Ļ�ѧ����ʽΪ��FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4��
=7mol������Feԭ���غ㣬����FeSO4�����ʵ���=1mol+7mol��2=15mol������Sԭ���غ㣬����H2SO4�����ʵ���=1mol��2+7mol��3-15mol=8mol��������ԭ���غ㣬��8molH2O�μӷ�Ӧ�����Ը÷�Ӧ�Ļ�ѧ����ʽΪ��FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4��
��4��FeCl3��ǿ�������Σ�ˮ��Һ�����ԣ���Na2S��Һ�μӵ�FeCl3��Һ�У��е��������ɣ���Ӧ�ķ���ʽ�ǣ�Na2S+2FeCl3=S+FeCl2+2NaCl��˵�������������������ԣ�Fe3+>S��Na2S��ǿ�������Σ�ˮ��Һ�Լ��ԣ���FeC13��Һ�μӵ�Na2S��Һ�У�������Ӧ��2FeC13+3Na2S=Fe2S3+6NaCl������Fe2S3������S��Fe(OH)3��˵������Fe3+��������Fe(OH)3>Fe2S3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��С��ͬѧ���Թ������⣨H2O2���ķֽⷴӦ��̽��Ӱ�컯ѧ��Ӧ���ʵ�������
��1������С����һ��̽�����ݣ���ش�������⣺
�����ڲ�ͬ��������10mL H2O2��ȡ150mLO2�����ʱ�䣨�룩
| 30% H2O2 | 15% H2O2 | 10% H2O2 | 5%H2O2 |
������������ | ��������Ӧ | ��������Ӧ | ��������Ӧ | ��������Ӧ |
���������� | 360 | 480 | 540 | 720 |
����������� | 10 | 25 | 60 | 120 |
�������̽������ʱ��С������������ЩӰ�췴Ӧ���ʵ�����
�ڴ�������Ʒ����У�����ѡһ����˵��С����̽�����ۣ�
��2������С������һ��̽�����ݣ���ش�������⣺
ʵ����� | MnO2״̬ | �۲��� | ��Ӧ����ʱ�� |
��MnO2����5mL5%����������Һ�У����� | ��ĩ״ | ���ҷ�Ӧ�������ǵ�ľ����ȼ | 3.5���� |
��״ | ��Ӧ���������Ǻ�����ľ��δ��ȼ | 30���� |
�ٱ�ʵ��ķ�Ӧԭ���ǣ��û�ѧ����ʽ��ʾ�� ��
�ڱ�ʵ���̽��Ŀ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͨ�����ʯ��ˮ������ʹ��Һ����ǵ��ǣ� ��
A.SO3B.O2C.SO2D.CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Pt�缫��⺬�и�0.1molCu2+��X3+����Һ�����������������ʵ�����m��g������Һ��ͨ�����ӵ����ʵ���n��mol���Ĺ�ϵ��ͼʾ�����������������ɴ�С������ȷ�� �� 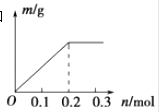
A.Cu2+��X3+��H+
B.H+��X3+��Cu2+
C.X3+��H+��Cu2+
D.Cu2+��H+��X3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж�����Ħ������������ȷ����( )
A. Ħ���ǹ��ʿ�ѧ�罨����õ�һ��������
B. 22.4LO2 ����������������Ϊ 1NA ��
C. 1mol ���� 6.02��1023 �� O2
D. Ħ�������ʵ����ĵ�λ�����Ħ������Ϊ mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ����·���ѩ���dz�ʹ��һ����ѩ��������Ҫ�ɷֵĻ�ѧʽΪXY2 �� X,Y��Ϊ���ڱ�ǰ20��Ԫ�أ��������Ӻ������ӵĵ��Ӳ�ṹ��ͬ����1mol XY2����54mol���ӣ�
����ѩ���Ļ�ѧʽ�� �� �������л�ѧ�������� �� ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50mL0.50mol��L��1��������50mL0.55mol��L��1������������Һ������ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⡣
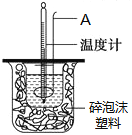
��1������A��������____________________________________��
��2��A�IJ����ܷ������ʵĴ��棿_______(������������������)����ԭ������________��
��3��ʵ��ʱ����������Һ��Ũ��Ҫ��0.55mol��L��1��ԭ������______________��
ʵ����������60mL0.5mol��L��1��������50mL0.55mol��L��1������������Һ���з�Ӧ��������ʵ����ȣ����ų�������________(��������������������)����ʵ���������ȷ���������к���________(��������������������)��
��4����֪��ϡ��Һ�У�ǿ���ǿ����кͷ�Ӧ����1molH2Oʱ���ų�57.3kJ����������������Ӧ���Ȼ�ѧ����ʽΪ��_________________________________________________��
��5������KOH����NaOH���Բⶨ���________(����������������)Ӱ�죻���ô������HCl��ʵ�飬�Բⶨ���________(����������������)Ӱ�졣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڳ����£�������Һ��������������ʢ�ŵ���
A. ����ͭ B. �������� C. Ũ���� D. ϡ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com