
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L的甲醇所含的氢原子数等于2NA | |
| B. | 常温常压下,Na2O2 与 H2O 反应生成 1mol O2 时,转移电子数是 2NA | |
| C. | 25℃时,Kap(BaSO4)=1×10-10,则BaSO4饱和溶液中Ba2+数目为1×10-6 NA | |
| D. | 1L 1 mol/L AlCl3溶液中含有的Al3+数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
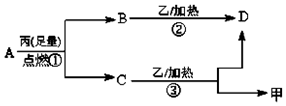 常温下,A是由X 和Y 两种短周期元素组成的气体,X的原子序数小于Y,甲、乙、丙分别是X、Y、Z元素对应的单质,Z是地壳中含量最高的元素,它们有如图所示的转化关系.下列说法不正确的是( )
常温下,A是由X 和Y 两种短周期元素组成的气体,X的原子序数小于Y,甲、乙、丙分别是X、Y、Z元素对应的单质,Z是地壳中含量最高的元素,它们有如图所示的转化关系.下列说法不正确的是( )| A. | X、Y、Z三种元素可能组成是离子化合物 | |
| B. | 反应②为化合反应,反应③为置换反应 | |
| C. | 常温常压下,Z的氢化物熔点为同族最高 | |
| D. | 原子半径:Y>Z>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeO与稀硝酸反应:FeO+2H+═Fe2++H2O | |
| B. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-═Fe(OH)2↓ | |
| C. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | |
| D. | 向碳酸钠溶液中逐滴加入等体积等物质的量浓度的稀醋酸:CO32-+H+═HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成42.0LN2(标准状况) | |
| B. | 被氧化的N原子的物质的量为3.75mol | |
| C. | 有0.250mol KNO3被氧化 | |
| D. | 转移电子的物质的量为1.75mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2气体通入Ba(NO3)2溶液中 | B. | NO2气体通入FeSO4溶液中 | ||
| C. | H2S气体通入CuSO4溶液中 | D. | HC1气体通入NaSiO3溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用铝热反应焊接铁轨 | B. | 用稀盐酸除去水垢 | ||
| C. | 用胃舒平(氢氧化铝)治疗胃酸过多 | D. | 工业上煅烧石灰石制生石灰 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com