
| A、该溶液由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合而成 |
| B、该溶液由0.2 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液等体积混合 |
| C、在上述溶液中加入适量CH3COOH,可能使溶液中离子浓度大小改变为:c(Na+ )>c(CH3COO-)>c(H+)>c(OH-) |
| D、该溶液由0.1 mol/L的CH3COOH溶液与等物质的量浓度等体积的NaOH溶液混合而成 |


科目:高中化学 来源: 题型:
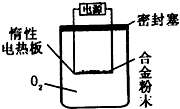
 铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某不同品牌铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某不同品牌铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.| 盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,下列说法中错误的是( )
,下列说法中错误的是( )| A、X可以是金属 |
| B、X可以是非金属 |
| C、m可以等于1或2 |
| D、XYm与XYn的相互转化是可逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将氨水逐滴滴加到AlCl3溶液中:Al3++3OH-=Al(OH)3↓ |
| B、铜与稀硝酸反应:Cu+4H++NO3-=Cu2++NO↑+2H2O |
| C、硫酸与氢氧化钡在溶液中反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、用FeCl3溶液腐蚀铜箔制造的印刷电路板:2Fe3++Cu=2Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A. | CO | CO2 | 通过足量氢氧化钠溶液,并干燥 |
| B. | H2 | 水蒸气 | 通过盛有浓硫酸的洗气瓶 |
| C. | N2 | O2 | 通过炽热的木炭 |
| D. | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用过滤的方法分离在一定量苯酚溶液中加入足量浓溴水后的混合物 |
| B、用加热的方法提纯含有少量碳酸钠的碳酸氢钠固体 |
| C、用溶解、过滤的方法提纯含有少量硫酸钡的碳酸钡 |
| D、用盐析的方法分离、提纯蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图里有6个编号,每个编号代表下列物质中的一种物质,凡用直线连接的相邻两种物质均能发生化学反应,供填写的物质有:a.碳酸钠溶液;b.硫酸镁溶液;C.氯化钡溶液;d.稀硫酸;e.铁;f.硝酸铜溶液,则图中③表示的物质的编号是( )
如图里有6个编号,每个编号代表下列物质中的一种物质,凡用直线连接的相邻两种物质均能发生化学反应,供填写的物质有:a.碳酸钠溶液;b.硫酸镁溶液;C.氯化钡溶液;d.稀硫酸;e.铁;f.硝酸铜溶液,则图中③表示的物质的编号是( )| A、e | B、f | C、a | D、d |
查看答案和解析>>
科目:高中化学 来源: 题型:
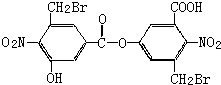
| A、该有机物的分子式为:C16H9O8N2Br2 |
| B、向该有机物溶液中加入FeCl3溶液,振荡后有紫色沉淀产生 |
| C、1mol该有机物与足量的NaOH溶液混合共热,充分反应最多可消耗6 mol NaOH |
| D、该有机物在稀硫酸中加热水解,有机产物只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
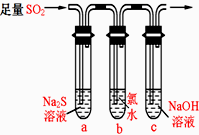 某学习小组设计用如下装置验证二氧化硫的化学性质.
某学习小组设计用如下装置验证二氧化硫的化学性质.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com