
【题目】根据下面的反应路线及所给信息填空
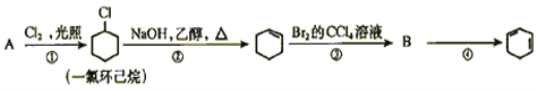
(1)A的名称是__________B的结构简式是_________
(2)②的反应类型是__________。③的反应类型是__________。
(3)反应④的化学方程式___________________。
【答案】环己烷 ![]() 消去反应 加成反应
消去反应 加成反应 ![]() +2NaOH
+2NaOH![]() +2NaBr+2H2O
+2NaBr+2H2O
【解析】
根据反应①的条件,A发生取代反应生成一氯环己烷,所以A是环己烷;一氯环己烷在氢氧化钠的乙醇溶液中发生消去反应生成环己烯,环己烯与溴的四氯化碳溶液发生加成反应生成B,则B是1,2-二溴环己烷;1,2-二溴环己烷在氢氧化钠的乙醇溶液中发生消去反应生成![]() 。
。
(1)A与氯气发生取代反应生成一氯环己烷,所以A是![]() ,名称是环己烷;环己烯
,名称是环己烷;环己烯![]() 与溴的四氯化碳溶液发生加成反应生成B,B的结构简式是
与溴的四氯化碳溶液发生加成反应生成B,B的结构简式是![]() ;
;
(2)②是一氯环己烷在氢氧化钠的乙醇溶液中发生反应生成环己烯,反应类型是消去反应。③是环己烯与溴的四氯化碳溶液发生反应生成![]() ,反应类型是加成反应。
,反应类型是加成反应。
(3)![]() 在氢氧化钠的乙醇溶液中发生消去反应生成
在氢氧化钠的乙醇溶液中发生消去反应生成![]() ,化学方程式是
,化学方程式是![]() +2NaOH
+2NaOH![]() +2NaBr+2H2O。
+2NaBr+2H2O。


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案科目:高中化学 来源: 题型:
【题目】NH4Cl是实验室常用试剂,下列相关说法正确的是
A.反应2NH4Cl(s)+Ba(OH)2(s)=BaCl2(s)+2NH3(g)+2H2O(s)的△H>0,△S<0
B.0.1mol·L-1NH4Cl溶液从15C升温到25°C时,![]() 的值不变
的值不变
C.反应NH4Cl+NaNO2=NaCl+N2↑+2H2O,每生成1molN2转移电子数为6×6.02×1023
D.常温下,Ksp[Mg(OH)2]=1.8x10-11,Kb(NH3·H2O)=1.8x10-5,NH4Cl饱和溶液中加入少量Mg(OH)2,振荡,固体逐渐溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g) +O2(g)=2H2O(g) ΔH =-483.6 kJmol-1
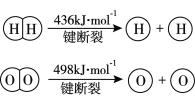
下列说法不正确的是
A. 该反应可作为氢氧燃料电池的反应原理
B. 破坏1mol H-O键需要的能量是463.4 kJ
C. H2O(g)=H2(g) +1/2O2(g) ΔH = +241.8 kJmol-1
D. H2(g)中的H-H键比H2O(g)中的H-O键牢固
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是2SO3(g)![]() 2SO2(g)+O2(g)的能量变化图,据图得出的相关叙述正确的是( )
2SO2(g)+O2(g)的能量变化图,据图得出的相关叙述正确的是( )
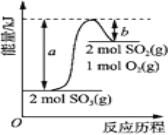
A. 该化学反应过程中既有能量的吸收又有能量的释放
B. 2SO3(g)![]() 2SO2(g)+O2(g) △H=-(a-b) kJ/mol
2SO2(g)+O2(g) △H=-(a-b) kJ/mol
C. 1 mol SO2的能量比1 mol SO3的能量高
D. 若某容器内有2 mol SO3充分反应,吸收(a-b) kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】补铁剂常用于防治缺铁性贫血,其有效成分一般为硫酸亚铁、琥珀酸亚铁、富马酸亚铁和乳酸亚铁等。回答下列问题:
(1)能表示能量最低的亚铁离子的电子排布式是_________(填标号)。
a.[Ar]3d54s2 b.[Ar]3d54s1 c.[Ar]3d64s2 d.[Ar]3d6
(2)琥珀酸即丁二酸(HOOCCH2CH2COOH),在琥珀酸分子中电负性最大的原子是_____,碳原子的杂化方式是______;琥珀酸亚铁中存在配位键,在该配位键中配位原子是____,中心原子是____。
(3)富马酸和马来酸互为顺反异构体,其电离常数如下表:
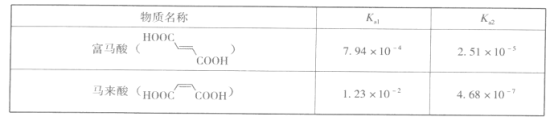
请从氢键的角度解释富马酸两级电离常数差别较小,而马来酸两级电离常数差别较大的原因:____。
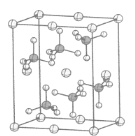
(4)β-硫酸亚铁的晶胞结构如图所示,其晶胞参数为a= 870 pm、b=680 pm、c=479 pm,α=β=γ=90°,Fe2+占据晶胞顶点、棱心、面心和体心。在该晶胞中,硫酸根离子在空间上有____种空间取向,晶胞体内硫酸根离子的个数是____,铁原子周围最近的氧原子的个数为____;设阿伏加德罗常数的值为NA,则该晶体的密度是____ g·cm-3(列出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设反应①Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数为K1;反应②Fe(s)+H2O(g)
FeO(s)+CO(g)的平衡常数为K1;反应②Fe(s)+H2O(g)![]() FeO(s)+H2(g)的平衡常数为K2。测得在不同温度下,K1、K2值如下:
FeO(s)+H2(g)的平衡常数为K2。测得在不同温度下,K1、K2值如下:
温度/℃ | K1 | K2 |
500 | 1.00 | 3.15 |
700 | 1.47 | 2.26 |
900 | 2.40 | 1.60 |
(1)若500 ℃时进行反应①,CO2的转化率为_______________。
(2)900 ℃时进行反应③H2(g)+CO2(g)![]() H2O(g)+CO(g),其平衡常数K3=______________。
H2O(g)+CO(g),其平衡常数K3=______________。
(3)反应②的焓变ΔH____________(填“>”、“<”或“=”)0。
(4)700 ℃时反应②达到化学平衡,要使该平衡向正反应方向移动,当其他条件不变时,可采取的措施有___________________________________。
A.缩小容器容积 B.加入更多的水蒸气
C.升高温度至900 ℃ D.使用合适的催化剂
(5)下列图像符合反应①的是________________________。
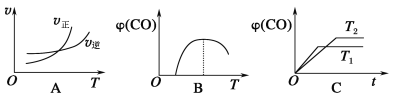
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应的叙述正确的是( )
A.SO2与Ba(NO3)2反应生成BaSO3
B.NH3在纯O2中燃烧生成NO2
C.过量CO2与氨水反应生成NH4HCO3
D.高温条件下Fe与水蒸气反应生成Fe(OH)3和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组对H2O2分解反应进行实验探究:将质量相等状态不同的MnO2分别加入盛有等体积等浓度的H2O2溶液的大试管中,并用带火星的木条在试管口测试。有关记录如下:
MnO2 | 触摸试管 | 现象 | 反应时间/min |
粉末 | 发烫 | 反应剧烈,带火星的木条迅速复燃 | t1 |
块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | t2 |
(1)试管中化学反应方程式:____________。
(2)实验结果证明了催化剂的催化效果与____________有关。
(3)表中t1____________t2(填写“>”、“<”或“=”)
(4)控制该反应速率,除了改变催化剂因素,可行的方法还有____________。
(5)某同学用一定浓度的H2O2溶液10mL,加入适量MnO2在某温度下反应,测量放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的即时反应速率最慢的是____________点。
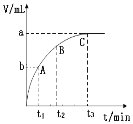
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,向20mL浓度均为0.1 mol·L-1的MOH和NH3·H2O混合液中滴加0.1mol·L-1的CH3COOH溶液,测得混合液的电阻率(表示电阻特性的物理量)与加入CH3COOH溶液的体积(V)的关系如图所示。已知CH3COOH的Ka=1.8×10-5,NH3·H2O的Kb =1.8×10-5。下列说法正确的是
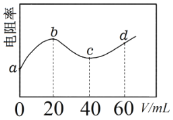
A.b→c过程发生的反应:MOH+CH3COOH=CH3COOM+H2O
B.c点溶液中:c(CH3COOH)+c(CH3COO–)=2c(NH4+)
C.d 点溶液中:c(CH3COO–)c(CH3COOH)>c(M+)>c(H+)>c(OH–)
D.a→c过程中水的电离程度一直在增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com