
【题目】氯酸镁常用作催熟剂、除草剂等,实验室制备Mg(ClO3)2·6H2O的流程如下:

已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S)随温度(T)变化曲线如图所示。

(1)加入NaClO3饱和溶液后发生反应的化学方程式为_______________,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:①_________;_____________;洗涤;②将滤液冷却结晶;③过滤、洗涤。
(2)产品中Mg(ClO3)2·6H2O含量的测定:(已知Mg(ClO3)2·6H2O的摩尔质量为299 g/mol)
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2:取10.00 mL于锥形瓶中,加入10.00 mL稀硫酸和20 .00 mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol/L K2Cr2O7溶液滴定剩余的Fe2+至终点。反应的方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00 mL。
①写出步骤2中发生反应的离子方程式____________________;
②产品中Mg(ClO3)2·6H2O的质量分数为________________。
【答案】 MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓ 蒸发浓缩或蒸发结晶 趁热过滤 ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O 78.3%
【解析】(1)向滤液中加入NaClO3饱和溶液后,发生反应MgCl2+2NaClO3=Mg(ClO3)2+2NaCl,然后利用NaCl、Mg(ClO3)2的溶解度与温度的关系将溶液蒸发浓缩结晶、②趁热过滤,③冷却结晶,最后④过滤、洗涤。就得到Mg(ClO3)2·6H2O。
(2)①步骤2中发生反应的离子方程式ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O,②在氧化反应反应中电子转移数目相等。n(Fe2+)×1=n(ClO3-)×6+n(Cr2O72-)×2×3. n(Fe2+)="0.02mol;" n(Cr2O72-)=0.0015mol;所以n(ClO3-)={0.02mol×1-0.0015mol×2×3}÷6=0.0018mol;因此100ml中含有的ClO3-的物质的量为0.0183mol,则含有的Mg(ClO3)2·6H2O的物质的量为0.00915mol.去质量为299g/mol×0.00915mol=2.7408g.因此产品中Mg(ClO3)2·6H2O的质量分数为(2.7408g÷3.50 g)×100%=78.3%.


科目:高中化学 来源: 题型:
【题目】下列实验中均需要的仪器是( )
①配制一定物质的量浓度的溶液 ②PH试纸的使用 ③过滤 ④蒸发
A. 试管 B. 胶头滴管
C. 玻璃棒 D. 漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的说法正确的是( )
A.Na2O、MgO、Al2O3均属于碱性氧化物
B.根据酸分子中含有的氢原子个数可将酸分为一元酸、二元酸、三元酸等
C.钠钾合金、铝热剂、氢氧化铁胶体、漂白粉均为混合物
D.纯碱、熟石灰、醋酸、食盐水均为电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于卤代烃的叙述中正确的是( )
A.所有卤代烃都是难溶于水,比水重的液体
B.所有卤代烃在适当条件下都能发生消去反应
C.所有卤代烃都含有卤原子
D.所有卤代烃都是通过取代反应制得的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应△H最小的是( )
A.NaOH(aq)+ ![]() H2SO4(aq)═
H2SO4(aq)═ ![]() Na2SO4(aq)+H2O(l);△H1
Na2SO4(aq)+H2O(l);△H1
B.NaOH(aq)+ ![]() H2SO4(浓)═
H2SO4(浓)═ ![]() Na2SO4(aq)+H2O(l);△H4
Na2SO4(aq)+H2O(l);△H4
C.NaOH(aq)+HCl(aq)═NaCl(aq )+H2O(l);△H2
D.CH3COOH(aq)+NaOH(aq)═CH3COONa (aq )+H2O(l);△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有NH4HCO3和NaHSO3的混合物,某兴趣小组为测定其中NH4HCO3的含量,设计了用在混合物中加酸的实验方法来测定其质量分数。 (已知酸性KMnO4被SO2还原的反应原理:SO2+MnO4-+H2O→SO42-+Mn2++H+)回答以下问题:
(1)化学小组主要选用了下列药品和仪器进行实验。(图中每种仪器装置只选用了一次,铁架台等固定仪器未画出)
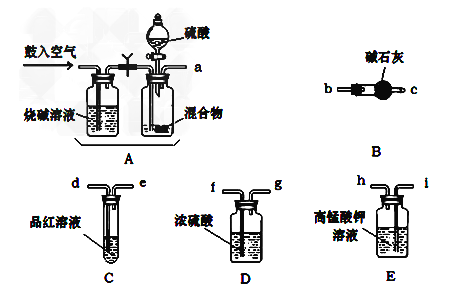
(1)请按气流由左向右的方向,仪器连接顺序是(填仪器的接口字母a、b…)
a→→_________________________________________。
(2)实验过程中空气的鼓入需要分2次,第一次鼓入空气的作用是_______________;
(3)C装置的作用是_________________。
(4)若混合物样品质量为13.1g,充分作用后碱石灰增重4.4g,则混合物中NH4HCO3的质量分数为____________。
(5)从定量测定的准确性考虑,该套装置还应作进一步的改进是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于乙酸的下列说法中不正确的是( )
A. 乙酸易溶于水
B. 无水乙酸又称冰醋酸,它是纯净物
C. 乙酸是一种重要的有机酸,是有刺激性气味的液体
D. 乙酸分子里有四个氢原子,所以不是一元酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分. 
(1)阴影部分元素N在元素周期表中的位置为 .
根据元素周期律,请你预测:H3AsO4、H3PO4的酸性强弱:H3AsO4H3PO4 . (用“>”、“<”或“=”表示)
(2)元素S的最高正价和最低负价分别为、 ,
(3)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下Se与H2反应的限度(选填“更大”、“更小”或“相同”) .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com