
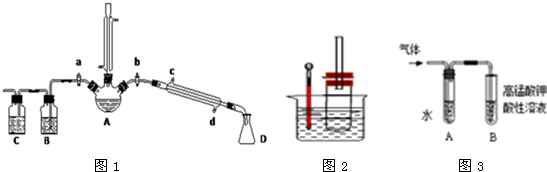
���� ��1���������ṹ������֪������A��������ƿ����ȡ����ԭ��ͨ������ˮ��
��2��Ũ�������ǿ�����ԣ����Խ�����������Ϊ�嵥�ʣ��Ʊ����������к���HBr�����������������Ȼ�̼�г�ȥ�壬��������������Һ����HBr��HBr��������ˮ��Cװ���е�����Һ��Ӵ���û������Һ�����£����Է�ֹ������
��3���������Ȼ�̼�г�ȥ�壬��������������Һ����HBr��
��4��Br2��NaI������ⵥ�����ʣ����������ƻ�����������ˮ�⣬�����Ȼ��ض�����Ӧ��
��5��ʵ������������ټ���������ˮ�ⷴӦ����Ӧ�����Ҵ���NaBr����Ӧ�����Һ���ٷֲ㣻
��6���Թ�A������ϩ�лӷ������Ҵ�����ֹ�����Ը��������Һ����������A�Թܣ�������ؿ���Ϊ��ˮ��
��� �⣺��1���������ṹ������֪������A��������ƿ����ȡ����ԭ��ͨ������ˮ����ֱ�����ܵĽ�ˮ����Ϊ�¿ڽ�����ֽ�������������
�ʴ�Ϊ��������ƿ���£�
��2��Ũ�������ǿ�����ԣ����Խ�����������Ϊ�嵥�ʣ��óȺ�ɫ���ʿ�����Br2���Ʊ����������к���HBr�����������������Ȼ�̼�г�ȥ�壬��������������Һ����HBr��HBr��������ˮ��Cװ���е�����Һ��Ӵ���û������Һ�����£����Է�ֹ������
�ʴ�Ϊ��Br2��C��
��3��B��ʢ�����Ȼ�̼�г�ȥ�壬C��ʢ����������Һ����HBr���ɣ�
�ʴ�Ϊ�����Ȼ�̼����������Һ��
��4��Br2��NaI������ⵥ�����ʣ����������ƻ�����������ˮ�⣬�����Ȼ��ض�����Ӧ��������������Һ��Ӧ���Ա���ȥ��
��ѡ��c��
��5��ʵ������������ټ���������ˮ�ⷴӦ����Ӧ�����Ҵ���NaBr��Һ�岻�ٷֲ㣬������������NaOH��Һ����ȫ��Ӧ��
�ʴ�Ϊ��Һ�岻�ֲ㣻
��6���Թ�A������ϩ�лӷ������Ҵ�����ֹ�����Ը��������Һ������Ӱ��Ӱ��ļ��飬����A�Թܣ�������ؿ���Ϊ��ˮ��
�ʴ�Ϊ�������Ҵ�����ˮ��
���� ���⿼���л����Ʊ�ʵ��������̽��ʵ�飬�ؼ��Ƕ�ԭ�����װ�õ����⣬����������ѧ������������ʵ�������������������������ȡ��±���������ʣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ƺϽ���۵������ | |
| B�� | ���ƺϽ���Ͷ��һ����ˮ�пɵ���ɫ��Һ����n��Al����n��Na�� | |
| C�� | ���ƺϽ�Ͷ�뵽�����Ȼ�ͭ��Һ�У��϶���������ͭ����Ҳ������ͭ���� | |
| D�� | m g��ͬ��ɵ����ƺϽ�Ͷ�����������У��ų���H 2 Խ�࣬��������������ԽС |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| 25��ʱ | pHֵ |
| ����H2S��Һ | 3.9 |
| SnS������ȫ | 1.6 |
| FeS��ʼ���� | 3.0 |
| FeS������ȫ | 5.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.25��b-2a��mol/L | B�� | 4��2a-b��mol/L | C�� | 2��b-2a��mol/L | D�� | 4��b-2a��mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
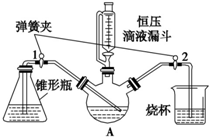 ij��ѧ��ȤС������ͼʵ��װ�ý��д����Ǹ����Ʊ��о�����֪�������Ǹ������и�Ԫ��Ϊ���ۣ��Ǻ���ɫ���壬������ˮ���ڳ�ʪʱ��Cr2+���ױ������� Cr3+������ע��Cr2+����Һ��Ϊ��ɫ����
ij��ѧ��ȤС������ͼʵ��װ�ý��д����Ǹ����Ʊ��о�����֪�������Ǹ������и�Ԫ��Ϊ���ۣ��Ǻ���ɫ���壬������ˮ���ڳ�ʪʱ��Cr2+���ױ������� Cr3+������ע��Cr2+����Һ��Ϊ��ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʹ�ô�����Ϊ�˼ӿ췴Ӧ���ʣ��������Ч�� | |
| B�� | �����ϵ�г���18O2��һ��ʱ���18Oֻ������SO3�� | |
| C�� | ����������������ڷ�Ӧ��������� | |
| D�� | ���÷�Ӧ��Ƴ�ԭ��أ��ų����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| CO2��g�� | H2��g�� | CO��g�� | H2O��g�� | |
| �� | a mol | a mol | 0 | 0 |
| �� | a mol | 2a mol | 0 | 0 |
| �� | a mol | a mol | 0 | a mol |
| �� | amol | amol | amol | amol |
| A�� | n��������n���ף���n���ң���n������ | B�� | n��������n���ף���n��������n���ң� | C�� | n��������n���ң���n��������n���ף� | D�� | n��������n���ң���n���ף���n������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
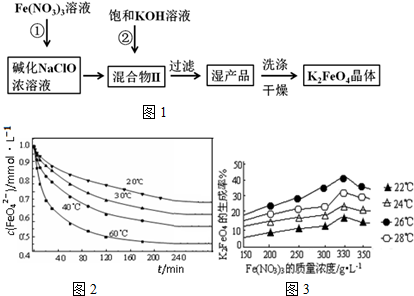
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X��Y��Z | B�� | Y��Z��X | C�� | X��Z��Y | D�� | Z��X��Y |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com