
掌握物质之间的转化,是学习元素化合物知识的基础。
(I)(1)中学常见的某反应的化学方程式为:
A+B→C+D+H2O(未配平,反应条件略去)。
若C、D均为气体,且都能使澄清石灰水变浑浊。
①请写出该反应的化学方程式____________;
②某探究性学习小组利用右图中所列装置实验,证明上述反应中有C、D生成。则b瓶溶液的作用是_________,该溶液还可以用_____________试剂代替。
③装置d中所盛溶液是__________。
(II)下列框图所示的物质转化关系中,甲、乙、丙是常见的气体单质。气体C与气体D相遇产生大量的白烟生成E,A是海水中浓度最高的盐(部分反应物和生成物及水已略
 去)。
去)。
请回答下列问题:
(1)写出C的电子式:___________________________。
(2)E是_______化合物(填“共价”或“离子”,含有的化学键为__________________。
(3)写出B和丙生成A的离子反应方程式_________________________________________。
(4)工业上可用C的浓溶液吸收某些工厂尾气中的SO2,写出反应成酸式盐的离子方程式:
______________________________________________________________________。
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
常温下,某未知溶液中 =1×1012,且含有大量Al3+和NO
=1×1012,且含有大量Al3+和NO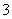 ,检验此溶液中是否大量存在以下6种离子:①SiO
,检验此溶液中是否大量存在以下6种离子:①SiO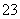 、②NH
、②NH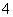 、③Fe2+、④Na+、⑤HCO
、③Fe2+、④Na+、⑤HCO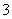 、⑥Cl-,其中不必检 验就能加以否定的离子是 ( )
、⑥Cl-,其中不必检 验就能加以否定的离子是 ( )
A.①③⑤ B.②③④ C.①②⑥ D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
已知: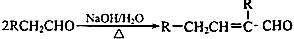 ;水杨酸酯E为紫外吸
;水杨酸酯E为紫外吸
收剂,可用于配制防晒霜。E的一种合成路线如下:
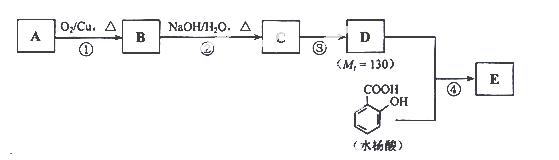
请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%。则A的分子式为 ;结构分析显示A只有一个甲基,A的名称为 。
 (2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为 。
(2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为 。
(3)C有 种结构;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂:
;
(4)第③的反应类型为 ;D所含官能团的名称为 。
(5)写出同时符合下列条件的水杨酸所有同分异构体的结构简式: 。
a.分子中含有6个碳原子在一条线上 b.分子中所含官能团包括水杨酸具有的官能团
(6)第④步的反应条件为 ;写出E的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中错误的是
A.氧化性;Na+<Mg2+<Al3+ B.半径:C1 >S2
>S2 >F
>F
C.稳定性:HF>HCl>HBr>HI D.酸性:HClO4>H2SO4>H2CO3>H2SiO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于某溶液所含离子检验的方法和结论正确的是
A.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,说明有Ca2+
B.通入少量Cl2后,溶液变为黄色,再加入淀粉溶液后,溶液变蓝,说明有I
C.加入盐酸产生能使澄清灰水变浑浊的气体,原溶液中一定有CO3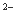 或SO
或SO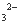
D.往溶液中加入BaCl2溶液和稀HNO3,有白色沉淀生成,说明一定有SO
查看答案和解析>>
科目:高中化学 来源: 题型:
亚硝酸(HNO2)在反应中既可作氧化剂,又可作还原剂。当它作氧化剂时,其还原产物可能是( )
①NO ②NO2 ③HNO3 ④N2 ⑤NH3
A.①③ B.①②④
C.①④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
已知: NO3-+4H++3e-→NO+2H2O 。现有四种物质:KMnO4、Na2CO3、Cu2O、Fe2(SO4)3,其中能使上述还原过程发生的是 (填化学式),写出该反应化学方程式中氧化产物的化学计量数(写方框内)及其化学式□ 。1mol该物质与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
1. 52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4 的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀
52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4 的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀 ,下列说法不正确的是
,下列说法不正确的是
A.该合金中铜与镁的物质的量之比是2 ︰1
B.该浓硝酸中HNO3的物质的量浓度是14.0mol/L
C.NO2和N2O4 的混合气体中,NO2 的体积分数是80%
D.得到2.54沉淀时,加入NaOH溶液的体积是600mL
查看答案和解析>>
科目:高中化学 来源: 题型:
容量瓶是用来配制一定物质的量浓度的溶液的定量仪器,其上标有①温度、②浓度、
③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的 ( )
A.②④⑥ B.③⑤⑥
C.①②④ D.①③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com