
| A. | 用惰性电极电解MgCl2 溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| B. | 1molN2与3molH2在某密闭容器中反应放出73kJ热量,则反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-73kJ/mol | |
| C. | 将AlCl3溶液与Na2S混合产生沉淀:2Al3++3S2-═Al2S3↓ | |
| D. | 2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H=-akJ•mol-1,则中和热为0.5akJ•mol-1 |
分析 A.电解生成氢氧化镁、氢气、氯气;
B.合成氨反应为可逆反应,热化学反应中为完全转化的能量变化;
C.发生相互促进水解反应;
D.酸与碱生成1mol水时的热量为中和热的数值.
解答 解:A.用惰性电极电解MgCl2 溶液的离子反应为Mg2++2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Mg(OH)2↓+H2↑+Cl2↑,故A错误;
B.1molN2与3molH2在某密闭容器中反应放出73kJ热量,若完全转化放出热量大于73kJ,则反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H<-73kJ/mol,故B错误;
C.将AlCl3溶液与Na2S混合产生沉淀的离子反应为2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑,故C错误;
D.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H=-akJ•mol-1,可知生成1mol水放出热量为0.5akJ,则中和热为0.5akJ•mol-1,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重电解、水解、热化学反应的离子反应考查,注意离子反应中保留化学式的物质和电荷守恒,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 常温时与锌反应生成大量氢气 | |
| B. | 置于敞口容器中,经过一段时间后质量将减少 | |
| C. | 常温时与铁、铝不反应 | |
| D. | 稀释时将浓硫酸沿器壁慢慢加到水中并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
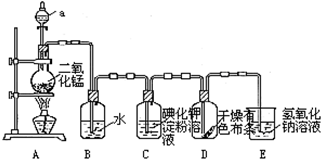
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
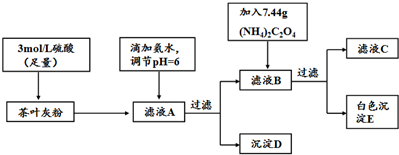
| 离子 | Ca2+ | Fe3+ |
| 完全沉淀时的pH | 13 | 3.7 |
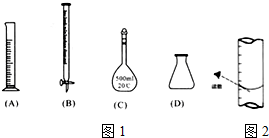
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某金属元素气态基态原子的逐级电离能的数值分别为738、1451、7733、10540、13630、17995、21703…,当它与氯气反应时生成的阳离子是X2+ | |
| B. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 | |
| C. | 标况下22.4LC2H2中所含的π键数和18g冰中所含的氢键数均为2mol | |
| D. | PCl5和AlCl3形成的加合物PCl5•AlCl3由[PCl4]+和[AlCl4]-构成,化合物中的阴阳离子均为正四面体构型 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在溴水中存在如下平衡:Br2+H2O=HBr+HBrO,当加入NaOH溶液后颜色变浅 | |
| B. | 对2HI?H2+I2(气)平衡体系增加压强使颜色变深 | |
| C. | 反应CO+NO2?CO2+NO+Q升高温度使平衡向逆方向移动 | |
| D. | 合成氨反应:N2+3H2?2NH3+Q,为使氨的产率提高,理论上应采取低温高压的措施 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可用作水果的催熟剂 | |
| B. | 二氧化硫可用作食品的漂白剂 | |
| C. | 交警可用酸性重铬酸钾来检测司机是否酒驾 | |
| D. | 黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com