
ijĶµÄŃõ»ÆĪļ¾§ĢåµÄ¾§°ū½į¹¹ČēĶ¼ĖłŹ¾£¬ĘäÖŠŠ”Ēņ±ķŹ¾CuŌ×Ó£¬ŌŚ1øö¾§°ūĖł°üŗ¬µÄŃõŌ×ÓŹżÄæĪŖ________£®

 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
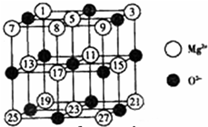 £Ø2008?¹ć¶«£©Ć¾”¢ĶµČ½šŹōĄė×ÓŹĒČĖĢåÄŚ¶ąÖÖĆøµÄøØŅņ×Ó£®¹¤ŅµÉĻ“Óŗ£Ė®ÖŠĢįČ”Ć¾Ź±£¬ĻČÖʱøĪŽĖ®ĀČ»ÆĆ¾£¬Č»ŗó½«ĘäČŪČŚµē½ā£¬µĆµ½½šŹōĆ¾£®
£Ø2008?¹ć¶«£©Ć¾”¢ĶµČ½šŹōĄė×ÓŹĒČĖĢåÄŚ¶ąÖÖĆøµÄøØŅņ×Ó£®¹¤ŅµÉĻ“Óŗ£Ė®ÖŠĢįČ”Ć¾Ź±£¬ĻČÖʱøĪŽĖ®ĀČ»ÆĆ¾£¬Č»ŗó½«ĘäČŪČŚµē½ā£¬µĆµ½½šŹōĆ¾£®| Ńõ»ÆĪļ | NaF | MgF2 | SiF4 |
| ČŪµć/K | 1266 | 1534 | 183 |
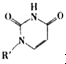 »ņCu£ØI£©£ØI±ķŹ¾»ÆŗĻ¼ŪĪŖ+1£©Ź±£¬·Ö±šŠĪ³ÉaŗĶb£ŗ
»ņCu£ØI£©£ØI±ķŹ¾»ÆŗĻ¼ŪĪŖ+1£©Ź±£¬·Ö±šŠĪ³ÉaŗĶb£ŗ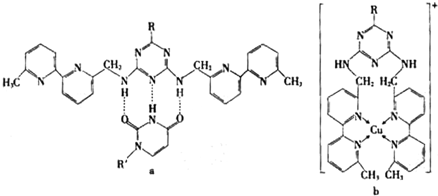
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 £Ø2010?ø§Ė³Ä£Äā£©£Ø1£©ĒėŠ“³öCrŌ×Ó»łĢ¬µÄµē×ÓÅŲ¼Ź½£ŗ
£Ø2010?ø§Ė³Ä£Äā£©£Ø1£©ĒėŠ“³öCrŌ×Ó»łĢ¬µÄµē×ÓÅŲ¼Ź½£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2009-2010Ń§ÄźÉ½¶«Ź”×Ķ²©ŹŠøßČż£ØÉĻ£©ĘŚÄ©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com