
| A. | 该反应中,铁元素的化合价由+3价升高到+6价 | |
| B. | 该反应涉及的物质都是氧化物 | |
| C. | 化学计量数m=n | |
| D. | 反应前后原子发生了改变 |
分析 A、化合物中元素化合价的代数和为零计算出Fe2O3中铁元素的化合价为+3价,生成物Na2FeO4中铁元素的化合价为+6价;
B、根据氧化物是由两种元素组成,其中一种元素为氧元素来判断;
C、根据质量守恒定律,反应前有2个铁原子,故n=2,则反应后钠的原子个数为6个,故m=3;
D、根据原子是化学变化中最小的粒子解答;
解答 解:A、该反应中,反应物Fe2O3中铁元素的化合价为+3价,生成物Na2FeO4中铁元素的化合价为+6价,故A正确;
B、氧化物是由两种元素组成,其中一种元素为氧元素,而方程式中Na2FeO4的组成元素有三种,故B错误;
C、根据质量守恒定律,反应前有2个铁原子,故n=2,则反应后钠的原子个数为6个,故m=3,故C错误;
D、原子在化学变化前后不会发生改变,故D错误;
故选A.
点评 本题考查化合价原则、氧化物定义以及质量守恒定律的内容,考查注重基础.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
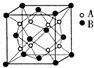 某离子晶体中晶体结构最小的重复单元如图:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体化学式可能为( )
某离子晶体中晶体结构最小的重复单元如图:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体化学式可能为( )| A. | CaF2 | B. | CaO2 | C. | CaC2 | D. | Na2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH分子中所有原子可能共平面 | |
| B. | 该反应能够发生是因为CH3COOH酸性比H2S酸性强 | |
| C. | H2S分子既存在极性键又存在非极性键 | |
| D. | 该反应每消耗4.8gSO42-,转移0.4NA个电子(NA为阿伏加德罗常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
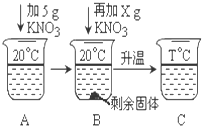 下表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:
下表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:| 温度(℃) | 10 | 20 | 40 | 60 | 80 |
| KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
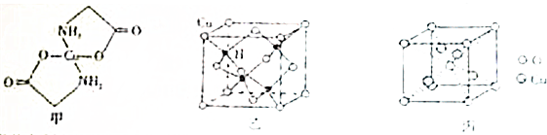
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C30、N70、C120、C340等互称为同素异形体 | |
| B. | CH3CH2CH2CH2OH的名称是:丁醇 | |
| C. | 2-戊烯的结构简式:CH3CH2CH=CHCH3 | |
| D. | 质子数为94、中子数为144的钚(Pu)原子:${\;}_{92}^{144}$Pu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乳酸薄荷醇酯(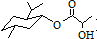 )只能发生水解、氧化、消去反应 )只能发生水解、氧化、消去反应 | |
| B. | 乙醛和丙烯醛不是同系物,它们的氢化产物也一定不是同系物 | |
| C. | 分子式为C7H14O2的有机物中,含3个甲基且能发生银镜反应还能发生水解反应的同分异构体数目是8个 | |
| D. | 硝化甘油、硝化纤维、硬脂酸甘油酯两两互不为同分异构体,其水解产物也完全不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{17}^{35}$Cl2与${\;}_{17}^{37}$Cl2氧化能力相近,二者互为同位素 | |
| B. | ${\;}_{34}^{78}$Se与${\;}_{34}^{80}$Se所含质子数相同,中子数不同 | |
| C. | 同主族元素形成的含氧酸的酸性随核电荷数的增加而减弱 | |
| D. | 同周期主族元素形成的简单离子半径随核电荷数的增大而减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com