
分析 (1)SO2与H2S反应,生成S与H2O;
(2)碳酸钡与盐酸反应生成氯化钡、二氧化碳与水;
(3)钝化是在金属表面生成一层致密的氧化物保护膜,阻止内部进行进行反应,若发生钝化,则氧化物保护膜阻止Fe与硫酸铜反应;
(4)根据二氧化硫和氢氧化钡的反应方程式进行计算,用CO还原SO2得到单质硫,根据电子转移守恒可知,碳元素被氧化生成二氧化碳.
解答 解:(1)SO2与H2S反应,二氧化硫中+4价的硫化合价降低,硫化氢中-2价的硫化合价升高,生成物在常温下均非气体,二者反应生成S与H2O,反应方程式为2H2S+SO2═2H2O+3S,
故答案为:2H2S+SO2═2H2O+3S;
(2)碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,奇反应的离子方程式为:BaCO3+2H+=Ba2++CO2↑+H2O;
故答案为:BaCO3+2H+=Ba2++CO2↑+H2O;
(3)钝化是在金属表面生成一层致密的氧化物保护膜,阻止内部继续进行反应,若发生钝化,则氧化镁保护膜阻止Fe与硫酸铜反应,无明显现象,否则发生反应,会有紫红色的铜析出,
故答案为:无明显现象(无现象也可);有红色物质析出;
(4)二氧化硫和氢氧化钡的反应方程式为:SO2+Ba(OH)2=BaSO3↓+H2O,设该雨水中共溶解SO2的体积是x,则
SO2 +Ba(OH)2=BaSO3↓+H2O
1 1
$\frac{x}{22.4L/mol}$0.5 mol/L×0.04L
则$\frac{x}{22.4}$=0.02,解得x=0.448L=448mL,
用CO还原SO2得到单质硫,根据电子转移守恒可知,碳元素被氧化生成二氧化碳,反应方程式:SO2+2CO $\frac{\underline{\;一定条件\;}}{\;}$ S+2CO2,
故答案为:448mL;SO2+2CO $\frac{\underline{\;一定条件\;}}{\;}$ S+2CO2.
点评 本题主要考查氧化还原反应、方程式的书写、元素化合物的性质等,题目难度中等,掌握元素化合物的性质是解题的关键,侧重于考查学生分析问题和解决问题的能力.


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:实验题
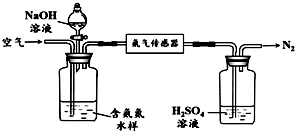

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
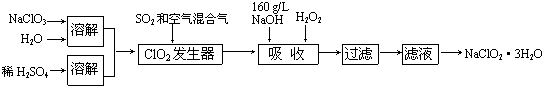
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl、SO3的水溶液均能导电,所以NaCl、SO3均为电解质 | |
| B. | 金属元素的原子只有还原性,其阳离子只有氧化性 | |
| C. | 用激光笔照射FeCl3溶液和Fe(OH)3胶体时,产生的现象不同 | |
| D. | 合金的硬度一般小于它的成分金属,熔点高于它的成分金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X为0.2 mol/L | B. | Y为0.1 mol/L | ||
| C. | Z为0.4 mol/L | D. | Z为0.1 mol/L时,Y为0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们都是天然高分子化合物 | B. | 油脂的水解产物是纯净物 | ||
| C. | 纤维素和淀粉遇碘水均显蓝色 | D. | 蛋白质水解的最终产物是氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解 | |
| B. | 用含硅胶、铁粉的透气小袋与食品一起密封包装 | |
| C. | H2、SO2、NH3三种气体都可用浓硫酸干燥 | |
| D. | SiO2既能和氢氧化钠溶液反应也能和氢氟酸反应,所以是两性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com