
| 1000ρω |
| M |
| n |
| V |
| 1000ρω |
| M |
| 1000×1.84g/ml×98% |
| 98g/mol |


科目:高中化学 来源: 题型:

| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mG | 255 | 385 | 459 |
| 气体休积/mL | 280 | 336 | 336 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,1 L0.1mol/LNa2CO3溶液中,含有阴离子的总数小于0.1 NA |
| B、常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4NA |
| C、5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等 |
| D、84 gNaHCO3与MgCO3的混合物中所含氧原子数目一定为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②①③④⑤ |
| B、①②③④⑤ |
| C、②③①④⑤ |
| D、②③①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④⑤⑥⑦⑧ | B、③④⑤⑥⑦⑧ |
| C、④⑤⑧ | D、④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯、聚乙烯均可使酸性KMnO4溶液褪色 |
| B、CCl4、苯均可用于萃取溴水中的溴 |
| C、乙醇、乙酸均可以发生取代反应 |
| D、多糖、油脂、蛋白质在一定条件下可发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
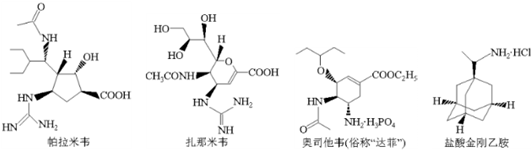
| A、帕拉米韦的分子式为C15H27N4O4 |
| B、扎那米韦与帕拉米韦的钠盐可用新制Cu(OH)2悬浊液鉴别 |
| C、1mol达菲最多能与5molNaOH反应 |
| D、盐酸金刚乙胺六元环上的一个氢原子被氯原子取代,所得一氯代物有三种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、既能溶解Al(OH)3,又能溶解H2SiO3的溶液:Na+、Fe2+、SO42-、Cl- |
| B、强碱性溶液中:Cl-、SO32-、HSO3-、Na+ |
| C、c(HCO3-)=0.1mol/L的溶液中:Na+、K+、CO32-、Br- |
| D、含有大量Fe3+的溶液:Na+、Al3+、NO3-、SCN- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com