
把含硫酸铵和硝酸铵的混合液a L分成两等份.一份加入含b mol NaOH的溶液并加热,恰好把NH3全部赶出;另一份需消耗c mol BaCl2才能使SO42﹣完全沉淀,则原溶液中NO3﹣的物质的量浓度为( )
A. 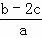 B.
B. 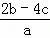 C.
C. 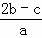 D.
D. 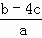
考点: 物质的量浓度的相关计算;离子方程式的有关计算.
专题: 计算题.
分析: bmol烧碱刚好把NH3全部赶出,根据NH4++OH﹣═NH3+H2O可知每份中含有bmolNH4+,与氯化钡溶液完全反应消耗cmolBaCl2,根据Ba2++SO42﹣═BaSO4↓可知每份含有SO42﹣cmol.根据溶液不显电性,计算出每份中NO3﹣的物质的量,再根据c= 计算.
计算.
解答: 解:bmol烧碱刚好把NH3全部赶出,根据NH4++OH﹣═NH3+H2O可知每份中含有bmolNH4+,
与氯化钡溶液完全反应消耗cmolBaCl2,根据Ba2++SO42﹣═BaSO4↓可知每份含有SO42﹣cmol.
令每份中NO3﹣的物质的量为n,根据溶液不显电性,则:
bmol×1=cmol×2+n×1
解得n=(b﹣2c)mol
每份溶液的体积为0.5aL,所以每份溶液硝酸根的浓度为c(NO3﹣)= =
= mol/L.
mol/L.
即原溶液中硝酸根的浓度为 mol/L.
mol/L.
故选B.
点评: 本题考查学生利用离子方程式的简单计算,关键明确每份溶液中离子的物质的量浓度与原溶液的关系及溶液中的电荷守恒.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
2014年1月初华北地区连续5~6天出现大雾,致使高速公路封闭、飞机停飞.雾属于下列分散系中的()
A. 胶体 B. 悬浊液 C. 溶液 D. 乳浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
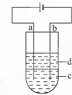
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.应用如下图所示电解实验可制得白色纯净的Fe(OH)2沉淀.两电极的材料分别为石墨和铁.
(1)a电极材料应为 ,电极反应式 ;
(2)电解液c可以是(填编号)
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用为 ,在加入苯之前对c应作怎样的简单处理? .
(4)为了在较短时间内看到白色沉淀,可采取的措施(填编号)
A.改用稀硫酸作电解液
B.适当增大电源的电压
C.适当减少两电极间距离
D.适当降低电解液的温度
(5)若c为Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一明显现象为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
镭是元素周期表中第七周期第ⅡA族元素,关于其叙述不正确的是( )
A. 镭的金属性比钙弱 B. 单质能与水反应生成H2
C. 在化合物中呈+2价 D. 碳酸镭难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
糖类物质为很多生物生命活动提供能量.
(1)已知 45g葡萄糖在人体内完全氧化为二氧化碳和水,放出701KJ的热量,该反应的热化学方程式 .
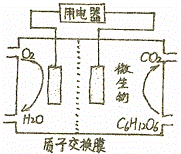
(2)以葡萄糖为燃料的微生物燃料电池结构如图所示,其负极反应为: .电池工作过程中溶液中氢离子移动方向从 极区移向 极区(填“正”或“负”)
(3)常温下,用上述电池惰性电极电解100L某浓的硫酸铜溶液,当溶液PH=1时停止电解,则理论上需要葡萄糖的质量为 (假设溶液体积不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是()
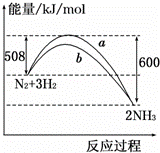
A. 该反应的热化学方程式为:N2+3H2⇌2NH3△H=﹣92 kJ/mol
B. a曲线是加入催化剂时的能量变化曲线
C. 加入催化剂,该化学反应的反应热改变
D. 在温度、体积一定的条件下,若通入2 mol N2和6 mol H2反应后放出的热量为Q kJ,则184>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,浓度都为1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z.反应2min后,测得 X2的浓度为0.4mol/L,用Y2的变化表示的反应速率v(Y2)=0.1mol/(L•min),生成的c(Z)=0.4mol/L,如z用X、Y表示,则该反应方程式是()
A. X2+2Y2═2XY2 B. 2X2+Y2═2X2Y C. 3X2+Y2═2X3Y D. X2+3Y2═2XY3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 在101kPa下,1g物质完全燃烧所放出的热量叫该物质的热值,单位为kJ•mol﹣1 |
|
| B. | 某放热反应在其它条件不变时,加入催化剂后反应放出的热量会减少 |
|
| C. | 一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的 |
|
| D. | 若一个反应的焓变△H=a kJ•mol﹣1,则其逆反应△H= |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com