
| A. | ②④⑤⑦ | B. | ②④⑥⑦ | C. | ①⑤⑥⑦ | D. | ②④⑥⑧ |
分析 水是一种弱电解质,存在电离平衡,影响水的电离平衡的因素主要有:温度,电离过程是吸热过程,升高温度促进电离;酸、碱抑制水的电离;能水解的弱碱阳离子、弱酸阴离子,促进水的电离;活泼金属促进水的电离,据此进行分析.
解答 解:水的电离平衡为:H2O?H++OH-,
①H+,加入氢离子,氢离子浓度增大,抑制了水的电离,故①错误;
②Cl-,加入氯离子,不影响水的电离,故②正确;
③Al3+,加入铝离子,能够结合水电离的氢氧根离子,促进了水的电离,故③错误;
④K+,加入钾离子,不影响水的电离,故④正确;
⑤SO42-,加入硫酸根离子,不影响水的电离,故⑤正确;
⑥OH-,加入氢氧根离子,溶液中的氢氧根离子浓度增大,抑制了水的电离,故⑥错误;
⑦NO3-,加入硝酸根离子,不影响水的电离,故⑦正确;
⑧NH4+,加入铵离子,铵离子结合水电离的氢氧根离子,促进了水的电离,故⑧错误;故选:A.
点评 本题考查了水的电离平衡,明确酸或碱能抑制水的电离、含有弱酸或弱碱离子的盐能促进水的电离是解本题关键,难度中等.


科目:高中化学 来源: 题型:选择题
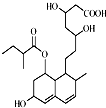 一种调节血脂的药物普伐他汀,其结构简式如图所示.下列有关普伐他汀说法正确的是( )
一种调节血脂的药物普伐他汀,其结构简式如图所示.下列有关普伐他汀说法正确的是( )| A. | 不能使酸性KMnO4溶液褪色,但能与FeCl3溶液发生显色反应 | |
| B. | 含有4种含氧官能团 | |
| C. | 能发生加成、取代、消去反应 | |
| D. | 1mol该物质最多可与5molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有机物A的分子式为C2H4,可能发生以下系列转化:
有机物A的分子式为C2H4,可能发生以下系列转化:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
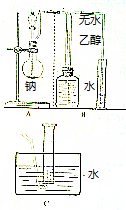 乙醇的分子式为C2H6O,有人设计了如图所示的实验来确定乙醇分子的结构.
乙醇的分子式为C2H6O,有人设计了如图所示的实验来确定乙醇分子的结构.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 | A | B | C | D | E | F | |
| 混 合 溶 液 | 4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 | |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 | |
| 时间(min) | 15 | 10 | 5 | 3 | 6 | 9 | |
| 实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
| , |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 杭州市萧山区红山农场近期完成了天然气管道安装,从此每家每户结束液化煤气使用时代,这一举措有利于降低氮氧化合物的排放 | |
| B. | 电动汽车、甲醇燃料汽车的出现,有利于节能减排,保护环境 | |
| C. | 利用天阳能等清洁能源代替化石燃料,有利于节约资源,造福后代 | |
| D. | 2015年春节期间,烟花爆竹的燃放时间比往年减少一天,市民也自觉减少烟花的燃放量,这有利于减少雾霾天气的出现 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一定温度和电压下,电解精制食盐水可制取NaClO3.电解装置如图.已知:3Cl2+6OH-=ClO3-+5Cl-+3H2O.下列说法正确的是( )
一定温度和电压下,电解精制食盐水可制取NaClO3.电解装置如图.已知:3Cl2+6OH-=ClO3-+5Cl-+3H2O.下列说法正确的是( )| A. | 铁为阳极,电极反应式为2H2O+2e-=H2↑+2OH- | |
| B. | 若阴极产生3.36L(标况)气体,则溶液中的反应转移电子0.30mol | |
| C. | 电解槽内总反应方程式为:NaCl+3H2O $\frac{\underline{\;通电\;}}{\;}$NaClO3+3H2↑ | |
| D. | 用阳离子交换膜代替阴离子交换膜,也一样可以制得NaClO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
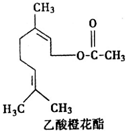
| A. | 分子式为C12H20O2 | |
| B. | 能使酸性KMnO4溶液褪色 | |
| C. | 能发生加成反应,但不能发生取代反应 | |
| D. | 1mol该有机物水解时只能消耗lmolNaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com