



 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、常温下pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
| B、用饱和Na2CO3溶液处理BaSO4沉淀,可将BaSO4转化为BaCO3 |
| C、BaSO4(s)+4C(s)═BaS(s)+4CO(g)室温下不能自发进行,说明该反应的△H<0 |
| D、为准确测定盐酸与氢氧化钠溶液反应的中和热,所用酸和碱的物质的量应相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.015mol?L-1 |
| B、0.011mol?L-1 |
| C、0.00751mol?L-1 |
| D、0.00251mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
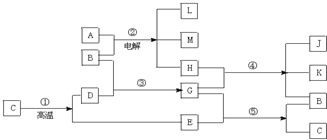
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铅笔芯的主要成分是金属铅,儿童在使用是不可用嘴吮吸,以免引起铅中毒 |
| B、CO有毒,在生有炉火的居室中多放几盆水,可吸收CO,防止煤气中毒 |
| C、含氟冰箱产生的氟利昂是造成臭氧空洞的主要原因 |
| D、油条制作中常加入明矾作膨化剂,有利于补充身体所需微量元素,是理想早餐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该合金中铜与镁的物质的量之比是2:1 |
| B、得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL |
| C、NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D、该浓硝酸中HNO3的物质的量浓度是14.0 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
 钠型离子交换剂磺化煤(NaR)可使硬水的Ca2+、Mg2+通过离子交换而软化.现代海水的淡化方法是使海水(含Na+、Mg2+、Ca2+、Cl-等)依次通过两种离子交换树脂A、B(如图所示),下列说法不正确的是( )
钠型离子交换剂磺化煤(NaR)可使硬水的Ca2+、Mg2+通过离子交换而软化.现代海水的淡化方法是使海水(含Na+、Mg2+、Ca2+、Cl-等)依次通过两种离子交换树脂A、B(如图所示),下列说法不正确的是( )| A、A为氢型阳离子交换树脂(HR),B为羟型阴离子换树脂(ROH) |
| B、A为羟型阳离子交换树脂(ROH),B为氢型阳离子交换树脂(HR) |
| C、HR与Na+的反应可表示为HR+Na+═NaR+H+ |
| D、由中性海水用此方法得到的淡水pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某烷烃的名称为2,2,4,4-四甲基-3,3,5-三乙基己烷 |
B、化合物 在酸性条件下水解,所得溶液加碱后加热有NH3生成 在酸性条件下水解,所得溶液加碱后加热有NH3生成 |
C、 可由其单体通过缩聚反应生成 可由其单体通过缩聚反应生成 |
| D、等质量的甲醛与乳酸[CH3CH(OH)COOH]完全燃烧消耗氧气的量不相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com