
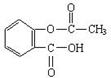
 化学是造福人类的科学,在人体保健、医疗卫生等方面作出了重大的贡献.请你用所学的化学知识解答有关问题.
化学是造福人类的科学,在人体保健、医疗卫生等方面作出了重大的贡献.请你用所学的化学知识解答有关问题.| 78 |
| 0.195 |
| 3 |
| X |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
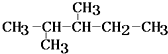
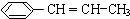 )在催化剂作用下生成聚苯丙烯的反应方程式:
)在催化剂作用下生成聚苯丙烯的反应方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 加热 |
| 温度℃ | 450 | 500 | 550 | 600 |
| SO2的转化率% | 97.5 | 95.8 | 90.50 | 80.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
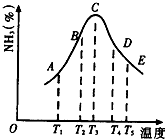 (1)在容积不同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2+3H2?2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如图所示:
(1)在容积不同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2+3H2?2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如图所示:| 物质 | N2 | H2 | NH3 |
| 起始浓度(摩/升) | a | 6 | 0 |
| 转化浓度(摩/升) | b | c | d |
| 平衡浓度(摩/升) | 1 | e | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
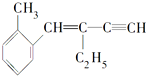
| A、该有机物分子式为C13H16 |
| B、该有机物属于苯的同系物 |
| C、该有机物分子至少有4个碳原子共直线 |
| D、该有机物分子最多有13个碳原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3胶体带正电荷 |
| B、胶体是一种不稳定的分散系 |
| C、当光束通过硫酸铜溶液时,能观察到丁达尔效应 |
| D、溶液和胶体中的粒子都能够透过滤纸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com