
| A. | “地沟油”经过加工处理后,可以用来制肥皂 | |
| B. | 二氧化硫有漂白性,常用作棉、麻、纸张和食品的漂白 | |
| C. | 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 | |
| D. | 含磷污水是很好的肥料,可灌溉庄稼,可直接排放到自然界水体中 |
分析 A.地沟油属于油脂,油脂可发生皂化反应制肥皂;生物柴油是以动植物油脂、废餐饮用油等为原料与甲醇在催化剂作用下,进行酯交换制成的液体燃料;
B.二氧化硫有毒,不能漂白食品;
C.汽车尾气污染物中含有氮的氧化物,是空气中的氮气在(发动机)高温条件下生成的;
D.直接排放含磷污水会造成水体富营养化.
解答 解:A.地沟油经过皂化反应制肥皂,与甲醇在催化剂作用下进行酯交换制成生物柴油,故A正确;
B.二氧化硫有漂白性,常用作棉、麻、纸张,但是二氧化硫有毒,不能漂白食品,故B错误;
C.汽车尾气排放的氮氧化物是在汽车发动机气缸内高温富氧环境下氮气和氧气的反应,不是汽油不完全燃烧造成的,故C错误;
D.含磷的污水虽然是很好的肥料,水中含量过高时会造成水体富营养化,致使水生藻类大量繁殖,由于水中缺氧造成水中生物大量死亡,遗体腐败,水质恶化,所以不能直接排放,故D错误;
故选A.
点评 本题考查化学与科学、技术、社会、环境等问题,题目难度不大,明确常见环境污染及治理措施为解答关键,试题侧重对基础知识的巩固,培养了学生的分析能力及灵活应用能力.


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:选择题
| A. | C70与金刚石一样属于原子晶体 | |
| B. | 共价化合物中一定不含离子键 | |
| C. | I2升华破坏了共价键 | |
| D. | HCl溶于水能电离子出H+、Cl-,所以HCl是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定容时仰视刻度线 | |
| B. | 定容后摇匀、静置,发现液面低于刻度线,又加水至刻度线 | |
| C. | 烧杯中的溶液未冷却至室温就将溶液移到容量瓶中 | |
| D. | 容量瓶洗涤后仍有少量残留 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
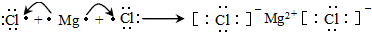 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水要现用现制,并保存在盖有橡胶塞的棕色瓶子中,置于冷暗处 | |
| B. | HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 | |
| C. | 向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 | |
| D. | 电解NaCl溶液得到22.4 L H2(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥⑦ | B. | ②⑤⑦⑧ | C. | ①③⑤⑥ | D. | ②⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 2:1:13 | C. | 13:1:2 | D. | 1:16:14 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com