
(1)将少量镁粉加入到氯化铁溶液中,有何现象?
;
有关的离子方程式
;
(2)将少量镁粉加入到氯化铵溶液中,有何现象?
有关的离子方程式
(1)镁粉不断溶解,溶液颜色变浅, 有大量气体和红褐色沉淀生成,
Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+ ,
Fe(OH)3 + 3H+ ,
2H+ +Mg =Mg2+ + H2↑;
2Fe3++3Mg=3Mg2++2 Fe2+
(因在FeCl3 溶液中Fe3+ 发生了如下水解:Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+ ,向其中加入Mg粉后,Mg粉与 H+ 反应产生H2 ,从而打破解了高考资源网其水解平衡,使水解平衡向正向移动,就产生了红褐色的Fe(OH)3沉淀。)
Fe(OH)3 + 3H+ ,向其中加入Mg粉后,Mg粉与 H+ 反应产生H2 ,从而打破解了高考资源网其水解平衡,使水解平衡向正向移动,就产生了红褐色的Fe(OH)3沉淀。)
(2)镁粉不断溶解,有大量气体及白色沉淀产生。
NH4+ + H2O ![]() NH3 ?H2O + H+ ;
NH3 ?H2O + H+ ;
2H+ +Mg =Mg2+ + H2↑;
Mg2+ + 2NH3?H2O = Mg(OH)2↓+ 2NH4+ 。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
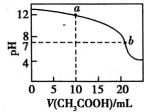 常温下有下列四种溶液:
常温下有下列四种溶液:| 序号 | ① | ② | ③ | ④ | 溶液 | pH=4的NH4Cl溶液 | pH=4的盐酸 | 0.1mol?L-1的醋酸溶液 | 0.1mol?L-1的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
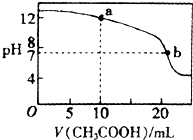 常温下有下列四种溶液:
常温下有下列四种溶液:| ① | ② | ③ | ④ | |
| 溶液 | pH=4的NH4Cl | pH=4的盐酸 | 0.1mol?L-1的醋酸 | 0.1mol?L-1的NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com