
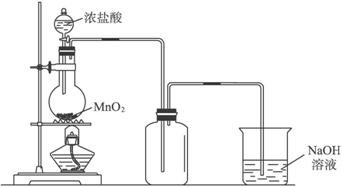
图4-3
(1)圆底烧瓶中发生反应的离子方程式:_______________________________________。
(2)如果将过量二氧化锰与20 mL 12 mol·L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06 mol。其主要原因有:
①_________________________________________________________________,
②_________________________________________________________________。
(3)为了提高浓盐酸的利用率,你对实验的建议是_____________________________________。
(4)实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是_____________,有关的离子方程式是_____________________________。
解析:(1)由制取Cl2的化学方程式:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,可知离子方程式为MnO2+4H++2Cl-
MnCl2+Cl2↑+2H2O,可知离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
(2)当20 mL 12 mol·L-1的盐酸完全反应产生氯气为0.06 mol,由于盐酸受热易挥发,且随着反应的不断进行,盐酸浓度越来越小,变为稀盐酸后不再与MnO2反应,所以产生氯气的物质的量小于0.06 mol。
(3)针对(2)中分析氯气减少的原因,可采取将浓盐酸慢慢滴入,用小火加热等措施,提高浓盐酸的利用率。
(4)选用碱液如NaOH溶液来吸收多余的氯气。
答案:(1)MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)加热使HCl大量挥发 盐酸变稀后不再发生反应
(3)将浓盐酸慢慢滴下;加热时用小火慢慢加热
(4)NaOH溶液 Cl2+2OH-====Cl-+ClO-+H2O


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:阅读理解
 Ⅰ.一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)
Ⅰ.一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g) FeO(s)+CO(g);△H>0
FeO(s)+CO(g);△H>0| c(CO) | c(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
一般情况下,较强的氧化剂如:MnO2、KMnO4、KClO3、Ca(ClO)2等氧化浓盐酸时,有如下反应规律:氧化剂+浓盐酸→金属氯化物+水+氯气。实验室通常用该原理制取少量Cl2。
⑴ 从原子经济学角度出发,要使浓盐酸中Cl-充分转化为Cl2,制取等量的Cl2最好选用上述氧化剂中的 氧化浓盐酸。
⑵ 将214.5gCa(ClO)2放入500 mL 、12.0 mol/L的浓盐酸中,生成的Cl2在标准状况下的体积为39.2 L。若反应前后溶液的体积保持不变,计算反应后溶液中HCl的物质的量浓度。
⑶ 漂白粉是 Ca(ClO)2、CaCl2 ?Ca(OH)2 ?H2O 和 CaO 的混合物。漂白粉放出的氯气具有漂白作用,叫有效氯。通常用有效氯表示漂白粉的纯度。漂白粉中的有效氯含量常用滴定碘法进行测定,即在一定量的漂白粉中加入过量的KI ,加H2SO4酸化,有效氯与I-作用析出等量的I2,析出的I2以淀粉指示剂立即用Na2S2O3标准溶液滴定。若测定漂白粉中有效氯时用盐酸酸化,则盐酸的浓度应小于 mol/L,否则测定的有效氯将 (“偏高”、“偏低”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com