
水解平衡右移,盐的离子的水解程度是否一定增大?
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
某校化学兴趣小组的同学对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定。请回答下列问题:
(1)甲同学运用沉淀法测定样品中NaOH的含量。该同学选用的药品除样品外,还应有________;实验中应测定的数据有________。
(2)乙同学运用滴定法测定样品中NaOH的含量。
①用分析天平准确称取该样品5.000 0 g,全部溶于水配制成1 000.0 mL溶液。用碱式滴定管量取20.00 mL所配溶液放在锥形瓶中,滴加几滴指示剂,待测。滴定管在使用前除洗涤外,还应____________________________________。
②用浓度为0.100 0 mol·L-1的盐酸标准溶液进行滴定。开始滴定前的一步操作是________。
③滴定过程中用pH计测定锥形瓶中溶液的pH,临近滴定终点时测定pH应每滴一滴测一次。
④滴定过程中,锥形瓶中溶液的pH变化如下:
| V(HCl)/mL | 0.00 | 12.00 | 18.00 | 22.00 | 23.00 | 23.96 | 24.00 | 24.04 | 25.00 | 26.00 | 30.00 |
| pH | 13.1 | 12.6 | 12.2 | 11.7 | 11.4 | 9.9 | 7.0 | 4.0 | 2.7 | 2.4 | 1.9 |
请在坐标图中绘制出上述中和滴定的曲线。

⑤如表所示是几种酸碱指示剂的变色范围,根据你所作的中和滴定曲线分析,上述中和滴定中应选用的指示剂是________。
| 指示剂 | 变色范围(pH) | 颜色 | |
| 酸 | 碱 | ||
| 甲基橙 | 3.1~4.4 | 红 | 黄 |
| 石蕊 | 5.0~8.0 | 红 | 蓝 |
| 酚酞 | 8.2~10.0 | 无 | 红 |
⑥样品中,NaOH的质量百分含量为____________。
答案 (1)MgCl2溶液 样品质量和加入足量MgCl2溶液后生成的沉淀质量
(2)①检漏、润洗 ②调节盛标准液的滴定管的液面于“0”刻度或“0”刻度以下
④滴定曲线如图所示
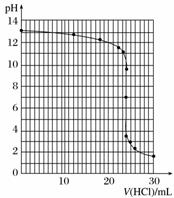
⑤甲基橙或酚酞 ⑥96%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.除0族元素外,短周期元素的最高化合价在数值上都等于该元素所属族的族序数
B.除短周期外,其他周期均为18种元素
C.副族元素没有非金属元素
D.碱金属元素是指ⅠA族(除H外)的所有的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学键的说法正确的是( )
A.构成单质分子的粒子中一定含有共价键
B.由非金属元素组成的化合物不一定是共价化合物
C.非极性键只存在于双原子单质分子里
D.不同元素组成的多原子分子中的化学键一定是极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
正误判断,正确的划“√”,错误的划“×”
(1)酸式盐溶液不一定呈酸性( )
(2)离子能够发生水解的盐溶液一定呈酸性或碱性( )
(3)同浓度的Na2CO3溶液和CH3COONa溶液相比前者pH大;同浓度的Na2CO3和NaHCO3溶液相比后者pH小( )
(4)常温下,pH=10的CH3COONa溶液与pH=4的NH4Cl溶液,水的电离程度相同( )
(5)常温下,pH=11的CH3COONa溶液与pH=3的CH3COOH溶液,水的电离程度相同( )
查看答案和解析>>
科目:高中化学 来源: 题型:
正误判断,正确的划“√”,错误的划“×”
(1)(2014·高考试题组合)
①施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用,是因为K2CO3与NH4Cl反应生成氨气会降低肥效( )
(2014·新课标全国卷Ⅰ,8C)
②小苏打是面包发酵粉的主要成分之一( )
(2014·福建理综,6D)
③将NH4Cl溶液蒸干制备NH4Cl固体( )
(2014·福建理综,8B)
④NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中( )
(2014·天津理综,3B)
(2)(2013·高考试题组合)
①向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成( )
(2013·重庆理综,2C)
②饱和小苏打溶液中:c(Na+)=c(HCO )( )
)( )
(2013·广东理综,12B)
③室温下,对于0.1 mol·L-1氨水,用HNO3溶液完全中和后,溶液不显中性( )
(2013·福建理综,8C)
④已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO +H2O??H2SO3+OH-①
+H2O??H2SO3+OH-①
HSO ??H++SO
??H++SO ②
②
向0.1 mol·L-1的NaHSO3溶液中
a.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO )增大( )
)增大( )
(2013·安徽理综,13A)
b.加入少量NaOH溶液,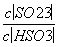 、
、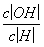 的值均增大( )
的值均增大( )
(2013·安徽理综,13C)
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH )________(填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH
)________(填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH )。
)。
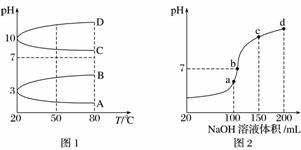
(2)如图1是0.1 mol·L-1电解质溶液的pH随温度变化的图像。
①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是________(填字母)。
②室温时,0.1 mol·L-1NH4Al(SO4)2中2c(SO )-c(NH
)-c(NH )-3c(Al3+)=________mol·L-1(填数值)。
)-3c(Al3+)=________mol·L-1(填数值)。
(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示:
试分析图中a、b、c、d四个点,水的电离程度最大的是____________;在b点,溶液中各离子浓度由大到小的排列顺序是________________________________。
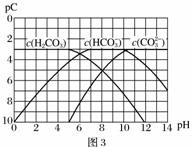
Ⅱ.pC是指极稀溶液中溶质物质的量浓度的常用对数负值,类似pH。如某溶液溶质的浓度为1×10-3mol·L-1,则该溶液中该溶质的pC=-lg10-3=3。已知H2CO3溶液中存在下列平衡:CO2+H2O??H2CO3、H2CO3??H++HCO 、HCO
、HCO ??H++CO
??H++CO
图3为H2CO3、HCO 、CO
、CO 在加入强酸或强碱溶液后,达到平衡时溶液中三种成分的pCpH图。请回答下列问题:
在加入强酸或强碱溶液后,达到平衡时溶液中三种成分的pCpH图。请回答下列问题:
(1)在pH=9时,H2CO3溶液中浓度最大的含碳元素的离子为______。
(2)pH<4时,溶液中H2CO3的pC总是约等于3的原因是____________________。
(3)已知M2CO3为难溶物,则其Ksp的表达式为______;现欲将某溶液中的M+以碳酸盐(Ksp=1×10-12)的形式沉淀完全,则最后溶液中的CO 的pC最大值为______(溶液中的离子浓度小于1×10-5mol·L-1时,沉淀完全)。
的pC最大值为______(溶液中的离子浓度小于1×10-5mol·L-1时,沉淀完全)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com