
【题目】有四种化合物W、X、Y、Z,它们都是由短周期元素A、B、C、D、E中的两种元素组成的.已知: (a)A、B、C、D、E五种元素的原子序数依次增大,且A、D同主族,C、E同主族,B、C同周期.
(b)W由B、C组成,分子中原子个数比为B:C=1:2,固体易升华.
(c)X由A、C组成,分子中原子个数比为A:C=1:1.
(d)Y由C、D形成的离子化合物,且Y中相应元素的微粒之比为:C:D=1:1.
(e)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阴、阳离子数之比为1:2.
试回答下列各小题:
(1)各元素符号:ABCDE
(2)W的电子式: .
(3)X的结构式: .
(4)Y的电子式: .
(5)Z的化学式: .
(6)写出Y与水反应的化学方程式: .
【答案】
(1)H;C;O;Na;S
(2)![]()
(3)H﹣O﹣O﹣H
(4)![]()
(5)Na2S
(6)2Na2O2+2H2O═4NaOH+O2↑
【解析】解:四种化合物W、X、Y、Z.它们都是由短周期元素A、B、C、D、E中两种元素组成,A、B、C、D、E五种元素的原子序数依次增大,且A、D同主族,C、E同主族,只能是A处于第一周期,C处于第二周期、D、E处于第三周期,则A为H元素,D为Na;Z是由D、E形成的离子化合物,E形成阴离子,其中阳离子比阴离子少一个电子层,阴、阳离子数之比为1﹕2,则E形成的阴离子带2个单位负电荷,所以E是S元素,则Z是Na2S;C和E同主族,所以C是O元素;X由A、C组成,分子中原子个数比A﹕C=1﹕1,则X是H2O2;Y是由C、D形成的离子化合物,且Y中相应元素的微粒之比为C:D=1:1,则Y是Na2O2;B、C同周期,W由B、C组成,分子中原子个数比为B:C=1:2,固体易升华,则B为碳元素,W为CO2 . (1)通过以上分析知,A、B、C、D、E分别是:H、C、O、Na、S 元素,故答案为:H;C;O;Na;S;(2)W为CO2 , 电子式为: ![]() ,故答案为:
,故答案为: ![]() ;(3)X是H2O2 , 结构式为:H﹣O﹣O﹣H,故答案为:H﹣O﹣O﹣H;(4)Y为Na2O2 , 电子式是:
;(3)X是H2O2 , 结构式为:H﹣O﹣O﹣H,故答案为:H﹣O﹣O﹣H;(4)Y为Na2O2 , 电子式是: ![]() ,故答案为:
,故答案为: ![]() ;(5)Z的化学式:Na2S,故答案为:Na2S;(6)Y与水反应的化学方程式:2Na2O2+2H2O═4NaOH+O2↑,故答案为:2Na2O2+2H2O═4NaOH+O2↑.
;(5)Z的化学式:Na2S,故答案为:Na2S;(6)Y与水反应的化学方程式:2Na2O2+2H2O═4NaOH+O2↑,故答案为:2Na2O2+2H2O═4NaOH+O2↑.
四种化合物W、X、Y、Z.它们都是由短周期元素A、B、C、D、E中两种元素组成,A、B、C、D、E五种元素的原子序数依次增大,且A、D同主族,C、E同主族,只能是A处于第一周期,C处于第二周期、D、E处于第三周期,则A为H元素,D为Na;Z是由D、E形成的离子化合物,E形成阴离子,其中阳离子比阴离子少一个电子层,阴、阳离子数之比为1﹕2,则E形成的阴离子带2个单位负电荷,所以E是S元素,则Z是Na2S;C和E同主族,所以C是O元素;X由A、C组成,分子中原子个数比A﹕C=1﹕1,则X是H2O2;Y是由C、D形成的离子化合物,且Y中相应元素的微粒之比为C:D=1:1,则Y是Na2O2;B、C同周期,W由B、C组成,分子中原子个数比为B:C=1:2,固体易升华,则B为碳元素,W为CO2 , 据此解答.


科目:高中化学 来源: 题型:
【题目】医学上最近合成一种具有抗癌活性的化合物,该物质结构简式为 ![]() 下列关于该化合物的说法正确的是( )
下列关于该化合物的说法正确的是( )
A.分子式为C12H19O4
B.是乙醇的同系物
C.可发生氧化反应
D.处于同一平面的原子最多有5个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是由Emil Zmaczynski设计的金字塔式元素周期表的一部分,图上标有第ⅥA族和几种元素的位置。请回答下列问题:

(1)铁元素位于元素周期表中第四周期__________族。
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,理由是氢原子的最外层电子“饱和缺一”。请写出LiH的电子式_____________,而且Li+的离子半径比H-_______(填“大”或“小”)。
(3)d的某化合物呈淡黄色,可与硫酸亚铁溶液反应生成红褐色沉绽和能使带火星的木条复燃的气体,d的该化合物中含有的化学键类型为__________________。
(4)b元素的氢化物与其最高价氧化物的水化物可生成一种盐,土壤中施用该盐做化肥时,其阴离子在水田中的利用率低,说明土壤胶体粒子带______(填“正”或“负”)电荷。
(5)下列叙述正确的是______
A.h的最高价氧化物对应的水化物是一种强碱
B.硒化氢的稳定性强于f的氢化物的稳定性
C.c的氢化物的水溶液是强酸
D.原子半径:h>e>a
E.氢化物的酸性:f弱于g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O(g)CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= , 该反应为反应(填吸热或放热). 若改变条件使平衡向正反应方向移动,则平衡常数(填序号)
①一定不变 ②一定减小 ③可能增大 ④增大、减小、不变皆有可能
(2)能判断该反应是否达到化学平衡状态的依据是 . (a)容器中压强不变 (b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O) (d)c(CO)=c(CO2)
(3)将不同量的CO (g) 和H2O (g) 分别通入到体积为2L的恒容密闭容器中,进行反应CO (g)+H2O (g)CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | CO2 | CO | |||
A | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
B | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
C | 900 | a | b | c | d | t |
①实验A中以υ(H2) 表示的反应速率为
②通过计算可知,CO的转化率实验A实验B(填“大于”、“等于”或“小于”),该反应的正反应为(填“吸”或“放”)热反应.
③若实验C要达到与实验B相同的平衡状态,则a、b应满足的关系是(用含a、b的数学式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学键的说法正确的是( )
A.在MgBr2晶体中既存在离子键又存在共价键
B.单质中均不存在化学键
C.离子键是阴、阳离子通过静电作用而形成的化学键
D.都由非金属元素组成的化合物里不可能存在离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷在高压下隔绝空气加热后急速冷却,可得钢灰色固体黑磷,其转化过程中能量变化如图所示.下列叙述中正确的是( ) 
A.黑磷比白磷稳定
B.黑磷与白磷互为同分异构体
C.白磷转化为黑磷是氧化还原反应
D.白磷转化为黑磷是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】马日夫盐是一种白色晶体,易溶于水,常用于机械设备的磷化处理.以软锰矿(主要成分为MnO2 , 还含有少量的Fe2O3、FeO和Al2O3)为原料制备马日夫盐的流程如图: 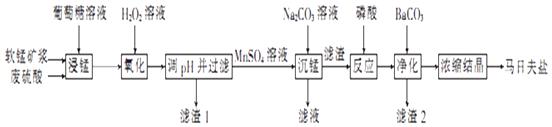
(1)软锰矿要先制成矿浆的目的是 , 葡萄糖(C6H12O6)与MnO2反应时,产物为MnSO4、CO2和H2O,该反应中氧化剂与还原剂的物质的量之比为 .
(2)用H2O2溶液“氧化”时发生反应的列子方程式为 .
(3)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如表所示、“调pH并过滤”时,应调整的pH范围为 , 滤渣1的主要成分为(填化学式).
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.8 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
Mn2+ | 7.8 | 9.8 |
(4)加入磷酸后发生反应的化学方程式为 .
(5)某工厂用上述流程制备马日夫盐,已知软锰矿中MnO2的含量为87%,整个流程中锰元素的损耗率为9%,则1t该软锰矿可制得马日夫盐t.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com