
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:选择题
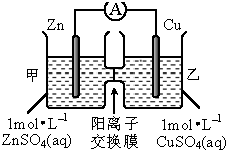
| A. | 锌电极上发生还原反应 | |
| B. | 电池工作一段时间后,甲池的c(SO42-)不变 | |
| C. | 电池工作一段时间后,甲池溶液的总质量增加 | |
| D. | 该装置将化学能转化为电能,一段时间后,装置内的电子总量减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 讨论 | B. | 调查 | C. | 观察和实验 | D. | 上网 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200mL O2 | B. | 150ml H2 | ||
| C. | 100mL H2和100mL F2 | D. | 150mL NH3和150mL HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 实验室中配制碘水,往往是将I2溶于KI溶液中,这样就可以得到浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-?I3-,上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任意一点都表示平衡状态).
实验室中配制碘水,往往是将I2溶于KI溶液中,这样就可以得到浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-?I3-,上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任意一点都表示平衡状态).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 根据图1可知合成甲醇的热化学方程式为CO(g)+2H2(g)═CH3OH(g)△H1=(b-a)kJ•mol-1 | |
| B. | 图2表示2 mol H2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ | |
| C. | 1 mol NaOH分别和1 mol 稀硫酸、1 mol浓硫酸反应,前者的△H比后者的△H大 | |
| D. | 汽油燃烧时将全部的化学能转化为热能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,Y、Z为同周期金属元素,Y、Z的最高价氧化物对应水化物可以反应生成盐和水.回答下列问题:
,Y、Z为同周期金属元素,Y、Z的最高价氧化物对应水化物可以反应生成盐和水.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com