
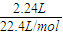 mol×4£¬
mol×4£¬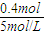 =0.08L=80mL£¬
=0.08L=80mL£¬


| Ä꼶 | ¸ßÖĐ¿Î³̀ | Ä꼶 | ³ơÖĐ¿Î³̀ |
| ¸ß̉» | ¸ß̉»Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ở» | ³ở»Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ß¶₫ | ¸ß¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ơ¶₫ | ³ơ¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ßÈư | ¸ßÈưĂâ·Ñ¿Î³̀ÍƼö£¡ | ³ơÈư | ³ơÈưĂâ·Ñ¿Î³̀ÍƼö£¡ |
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
| A¡¢½«0.1mol CuSO4?5H2O¾§̀å¼ÓÈëµ½100 mLË®ÖĐ£¬¸ĂÈÜ̉ºÎïÖʵÄÁ¿Å¨¶ÈΪ1 mol?L-1 | ||
| B¡¢̉»¶῭å»ưµÄŨẠ́ËᣨÆäÖĐº¬0.2mol H2SO4£©Óë×ăÁ¿µÄ͹²ÈÈ·´Ó¦£¬Éú³ÉSO2Æø̀å0.1mol | ||
| C¡¢½«34.2 g Al2£¨SO4£©3ÈÜÓÚË®Åä³É100 mLÈÜ̉º[Al2£¨SO4£©3µÄÏà¶ÔÖÊÁ¿Îª342J£¬È¡³ö10 mL¸ĂÈÜ̉ºÖĐAl3+Ũ¶ÈΪ1 mol?L-1 | ||
D¡¢KClÈÜ̉ºµÄĂܶÈΪ1.174 g?cm-3£¬ÎïÖʵÄÁ¿Å¨¶ÈΪ4.0 mol?L-1£¬Ộ´ËÈÜ̉ºÖĐKClµÄÖÊÁ¿·ÖÊưΪ
|
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£ºµ¥Ñ¡̀â
²é¿´´đ°¸ºÍ½âÎö>>
°Ù¶ÈÖÂĐÅ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com