
| A、ZnC2 |
| B、Al4C3 |
| C、Mg2C3 |
| D、Li2C2 |


科目:高中化学 来源: 题型:
| A、滴定时,装NaOH溶液的锥形瓶未用NaOH溶液润洗 |
| B、酸式滴定管用蒸馏水洗后,用标准盐酸润洗 |
| C、滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失 |
| D、配置NaOH溶液时,NaOH固体中混有少量KOH固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
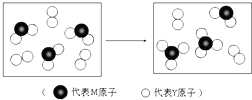
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 有关性质及结构信息 |
| A | A的一种原子内无中子 |
| B | B原子最外层电子数是内层电子数的2倍 |
| C | 一个C2-离子含10个电子 |
| D | A与D同族 |
| E | C与E同族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCOONa=NaCN |
| B、HCOONa>NaCN |
| C、HCOONa<NaCN |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将NaOH溶液逐滴滴入FeSO4溶液中,只观察到白色沉淀 |
| B、将钠放入水中,钠浮在水面上、熔成一个闪亮的小球、四处游动、溶液变红 |
| C、除去表面保护膜的铝在酒精灯上加热到熔化,熔化的铝以小液滴的形式滴落下来 |
| D、在滴有酚酞溶液的 Na2SiO3溶液中,逐滴加入稀盐酸,溶液的红色逐渐变浅,并有白色胶状物生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com