
乙酰基二茂铁是常用的汽油的抗震剂,由二茂铁合成乙酰基二茂铁的原理如下: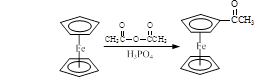
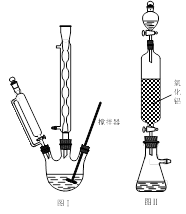
其实验步骤如下:
步骤1:如图Ⅰ所示,取1 g二茂铁与3 mL乙酸酐于装置中,开通搅拌器,慢慢滴加85%磷酸1 mL,加热回流5 min。
步骤2:待反应液冷却后,倒入烧杯中加入10 g碎冰,搅拌至冰全部融化,缓慢滴加NaHCO3溶液中和至中性,置于冰水浴中15 min。抽滤,烘干,得到乙酰基二茂铁粗产品。
步骤3:将乙酰基二茂铁粗产品溶解在苯中,从图Ⅱ装置的分液漏斗中滴下,再用乙醚淋洗。
步骤4:将其中一段时间的淋洗液收集,并进行操作X,得到纯净的针状晶体乙酰基二茂铁并回收乙醚。
(1)步骤2中的抽滤操作,除烧杯、玻璃棒外,还必须使用属于硅酸盐材质的仪器有 。
(2)步骤2中不需要测定溶液的pH就可以判断溶液接近中性,其现象是 。
(3)步骤3将粗产品中杂质分离实验的原理是 。
(4)步骤4中操作X的名称是 ,该操作中不能使用明火的原因是 。
(5)为确定产品乙酰基二茂铁中是否含有杂质二乙酰基二茂铁(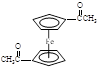 ),可以使用的仪器分析方法是 。
),可以使用的仪器分析方法是 。
(1)布氏漏斗、抽滤瓶
(2)滴加NaHCO3溶液不再产生气泡
(3)不同物质在扩散剂中扩散的速率不同
(4)蒸馏 乙醚易挥发且易燃
(5)质谱法或核磁共振氢谱
解析试题分析:(1)抽滤需使用的仪器有:布氏漏斗、抽滤瓶、胶管、抽气泵、滤纸、烧杯、玻璃棒等。其中属于硅酸盐材质的布氏漏斗、抽滤瓶、烧杯、玻璃棒。(2)碳酸氢钠溶液与酸不产生气体时即接近中性。(3)步骤3利用不同物质在扩散剂中扩散速率不同进行物质的分离。(4)步骤4将淋洗液蒸馏得到产品并回收乙醚,因乙醚易挥发且易燃,不能使用明火。(5)乙酰基二茂铁和二乙酰基二茂铁相对分子质量不同,可用质谱法测定相对分子质量;乙酰基二茂铁和二乙酰基二茂铁中氢原子环境不同,可分析核磁共振氢谱图判断其中是否含有杂质。
考点: 化学实验


科目:高中化学 来源: 题型:填空题
聚酯纤维是目前产量第一的合成纤维。它可通过如下路线合成:
已知:①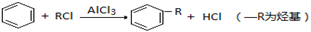
②
回答下列问题:
(1)若W的核磁共振氢谱显示有两个峰,峰值面积比是2 :3。
①W物质的结构简式为 。
②生成W的反应类型为 。
③J物质所含官能团的名称是 。
(2)若G的摩尔质量是116g/mol,其分子中含C为41.4%、含O为55.2%,其余为氢元素。下列叙述中不正确的有 。
a. A的同系物中可能存在顺反异构现象
b. 反应I需要在NaOH的乙醇溶液中完成
c. W与A均能使酸性KMnO4溶液褪色
d. 在B中滴加AgNO3溶液不会产生淡黄色沉淀
(3)完成化学方程式
①C→D: 。
②反应II: 。
③形成G: 。
(4)①J有多种同分异构体,满足以下条件J的同分异构体的个数是 ;
a.遇FeCl3溶液呈紫色; b.能发生银镜反应; c.1mol J能与最多3molNaOH反应;
②若1mol J最多能与4 molNaOH反应,写出J所有同分异构体的结构简式: 。
③生产中为提高产品质量,将粗品J溶于热水、过滤、 ,获得J的精品。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
制备苯乙酸的装置示意图如下(加热和夹持装置等略):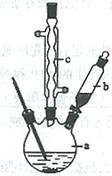
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是 。
(2)将a中的溶液加热至100 ℃,从b中缓缓滴加40 g苯乙腈( )到硫酸溶液中,然后升温至130 ℃继续反应。仪器c的名称是 ,反应结束后加适量冷水,再分离出苯乙酸(
)到硫酸溶液中,然后升温至130 ℃继续反应。仪器c的名称是 ,反应结束后加适量冷水,再分离出苯乙酸(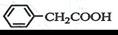 )粗品。加人冷水的目的是 。下列仪器中可用于分离苯乙酸粗品的是 (填标号)。
)粗品。加人冷水的目的是 。下列仪器中可用于分离苯乙酸粗品的是 (填标号)。
A 分液漏斗 B漏斗 C烧杯 D.直形冷凝管 E.玻璃棒
(3)提纯粗苯乙酸的方法是 ,最终得到44 g纯品,则苯乙酸()的产率是 。
(4)用CuCl2 ? 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是 。
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
【实验目的】制取乙酸乙酯
【实验原理】甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙 酸乙酯,该反应的化学方程式为 。
【装置设计】甲、 乙、丙三位同学分别设计了下列三套实验装置: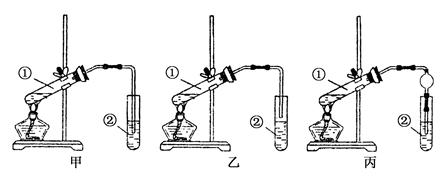
若从甲、乙两位同学设计的装置中选择一套作为实验室制取乙酸乙酯的装置,选择的装置应是 (填“甲”或“乙”)。丙同学将甲装置中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是 。
【实验步骤】
A 按所选择的装置组装仪器,在试管①中先加入3mL95%的乙醇,并在摇动下缓缓加入2 mL浓硫酸充分摇匀,冷却后再加入2 mL冰醋酸;
B 将试管固定在铁架台上;
C 在试管②中加入5 mL X试剂;
D 用酒精灯对试管①加热
E.当观察到试管②中有明显现象时停止实验。
【问题讨论】(1)实验中浓硫酸的作用是 。
(2)试管2中加入的X试剂为 。
(3)步骤E试管②中观察到的现象是 。
(4)常用 方法分离获得实验中的乙酸乙酯。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。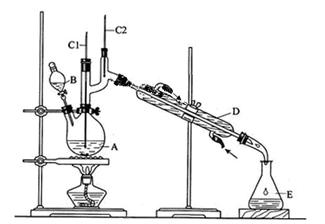
发生的反应如下: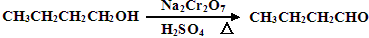
反应物和产物的相关数据列表如下:
| | 沸点/℃ | 密度/g·cm-3 | 水中溶解性 |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室可用环己醇(沸点:160.84℃,微溶于水)制备环己酮(沸点:155.6℃,微溶于水),使用的氧化剂可以是次氯酸钠、重铬酸钾等。
下列装置分别是产品的合成装置和精制装置示意图: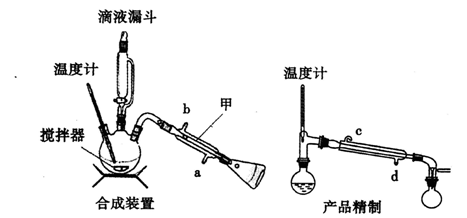
合成实验过程如下:
向装有搅拌器、滴液漏斗和温度计的三颈烧瓶中依次加入5.2 mL环己醇和25 mL冰醋酸。开动搅拌器,将40 mL次氯酸钠溶液逐渐加入到反应瓶中,并使瓶内温度维持在30~35℃,用磁性搅拌器搅拌5 min。然后,在室温下继续搅拌30 min后,在合成装置中再加入30 mL水、3g氯化铝和几粒沸石,加热蒸馏至馏出液无油珠滴出为止。
回答下列问题:
(1)在合成装置中,甲装置的名称是 。
(2)三颈烧瓶的容量为 (填“50 mL"、“100 mL”或“250 mL")。
(3)滴液漏斗具有特殊的结构,主要目的是____ 。
(4)蒸馏完成后,向馏出液中分批加入无水碳酸钠至反应液呈中性为止,其目的是 。然后加入精制食盐使之变成饱和溶液,将混合液倒人____ 中,分离得到有机层。
(5)用如上右图对粗产品进行精制,蒸馏收集____ ℃的馏分。
(6)检验坏己酮是否纯净,可使用的试剂为____ 。
A.重铬酸钾溶液 B.金属钠 C.新制的氢氧化铜悬浊液
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
苯酚具有弱酸性,在空气中易被氧化。工业上以苯、硫酸、氢氧化钠、亚硫酸钠为原料合成苯酚的方法可简单表示为: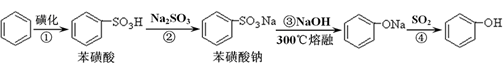
(1)根据上述反应判断下列三种物质的酸性由强到弱的顺序为 (填序号)。
A. B.
B.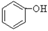 C.H2SO3
C.H2SO3
(2)步骤④与使用CO2相比,使用SO2的优点是 (答一个方面)。
(3)经反应④得到的产物除 外、可能还含有OH-、SO32-、HSO3-等微粒。请设计实验方案,证明溶液中存在
外、可能还含有OH-、SO32-、HSO3-等微粒。请设计实验方案,证明溶液中存在 、SO32-、HSO3-,写出实验步骤、预期现象和结论。
、SO32-、HSO3-,写出实验步骤、预期现象和结论。
限选仪器及试剂:试管、滴管、玻璃棒、过滤装置和滤纸;2mol·L-1盐酸、1mol·L-1 BaCl2溶液、品红溶液、0.01 mol·L-1酸性KMnO4溶液、1 mol·L-1 FeCl3溶液、饱和溴水等。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量待测液于试管中,加入足量的1 mol·L-1BaCl2溶液,静置、过滤,得滤液和沉淀。将滤液分置于试管A、B中,沉淀置于试管C中。 |  |
| 步骤2:往试管A中加入 。 | ,说明溶液中含有HSO3-。 |
| 步骤3:往试管B中加入 。 | 。 |
| 步骤4:往试管C中加入2 mol·L-1盐酸酸化,再滴入1~2滴品红溶液。 | ,说明溶液中含有SO32-。 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中,正确的是
| A.蛋白质遇硫酸钠溶液变性 | B.天然气的主要成分是甲烷 |
| C.涤纶、锦纶、蚕丝都属于合成纤维 | D.植物油不能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com