
| 离子 | SO42- | SO32- | NO3- | NO2- | Cl- |
| c/(mol•L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
分析 (1)NaClO2的化学名称为亚氯酸钠;
(2)①亚氯酸钠具有氧化性,则NaClO2溶液脱硝过程中主要反应的离子方程式为3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O;正反应是体积减小的,则增加压强,NO的转化率提高;
②根据反应的方程式3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O可知随着吸收反应的进行氢氧根离子被消耗,吸收剂溶液的pH逐渐降低;
③由实验结果可知,在相同时间内硫酸根离子的浓度增加的多,因此脱硫反应速率大于脱硝反应速率.原因是除了SO2和NO在烟气中的初始浓度不同,还可能是二氧化硫的还原性强,易被氧化;
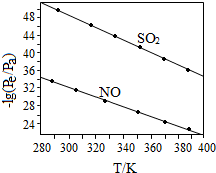
(3)①由图分析可知,根据反应3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O,NO的平衡分压的负对数随温度的升高而减小,则说明温度越高,NO的平衡分压越大,NO的含量越高,故升高温度,平衡向逆反应方向进行,平衡常数减小;
②根据反应的方程式ClO2-+2SO32-═2SO42-+Cl-可知平衡常数K表达式为K=$\frac{c(C{l}^{-}){c}^{2}(S{{O}_{4}}^{2-})}{c(Cl{{O}_{2}}^{-}){c}^{2}(S{{O}_{3}}^{2-})}$;
(4)①如果采用NaClO、Ca(ClO)2替代NaClO2,由于生成的硫酸钙微溶,降低硫酸根离子浓度,促使平衡向正反应方向进行;
②则根据盖斯定律计算.
解答 解:(1)NaClO2的化学名称为亚氯酸钠,故答案为:亚氯酸钠;
(2)①亚氯酸钠具有氧化性,且NaClO2溶液呈碱性,则NaClO2溶液脱硝过程中主要反应的离子方程式为3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O;正反应是体积减小的,则增加压强,NO的转化率提高,故答案为:3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O;提高;
②根据反应的方程式3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O可知随着吸收反应的进行氢氧根离子被消耗,吸收剂溶液的pH逐渐降低,故答案为:减小;
③由实验结果可知,在相同时间内硫酸根离子的浓度增加的多,因此脱硫反应速率大于脱硝反应速率.原因是除了SO2和NO在烟气中的初始浓度不同,还可能是NO溶解度较低或脱硝反应活化能较高,故答案为:大于;NO溶解度较低或脱硝反应活化能较高;
(3)①由图分析可知,根据反应3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O,NO的平衡分压的负对数随温度的升高而减小,则说明温度越高,NO的平衡分压越大,NO的含量越高,故升高温度,平衡向逆反应方向进行,平衡常数减小,故答案为:减小;
②根据反应的方程式ClO2-+2SO32-═2SO42-+Cl-可知平衡常数K表达式为K=$\frac{c(C{l}^{-}){c}^{2}(S{{O}_{4}}^{2-})}{c(Cl{{O}_{2}}^{-}){c}^{2}(S{{O}_{3}}^{2-})}$,故答案为:$\frac{c(C{l}^{-}){c}^{2}(S{{O}_{4}}^{2-})}{c(Cl{{O}_{2}}^{-}){c}^{2}(S{{O}_{3}}^{2-})}$;
(4)①如果采用NaClO、Ca(ClO)2替代NaClO2,生成硫酸钙沉淀,降低硫酸根离子浓度,促使平衡向正反应方向进行,所以Ca(ClO)2效果好,故答案为:形成CaSO4沉淀,反应平衡向产物方向移动,SO2转化率提高;
②已知SO2(g)+2OH-(aq)═SO32-(aq)+H2O(l)△H1
ClO-(aq)+SO32-(aq)═SO42-(aq)+Cl-(aq)△H2
CaSO4(s)═Ca2+(aq)+SO42-(aq)△H3
则根据盖斯定律可知①+②-③即得到反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)═CaSO4(s)+H2O(l)+Cl-(aq)△H=△H1+△H2-△H3.,故答案为:△H1+△H2-△H3.
点评 本题考查氧化还原反应、盖斯定律、外界条件对反应速率和平衡状态的影响等,要求学生掌握基本概念,结合生活实际分析问题、解决问题,方程式的书写要遵循相关守恒,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 16O2与18O2互为同素异形体 | |
| B. | Na2S的电子式为: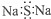 | |
| C. | 熔融状态下硫酸氢钾的电离方程式:KHSO4=K++H++SO42- | |
| D. | 钢铁表面常常出现的铁锈的主要成分是Fe2O3•xH2O,它不能阻止钢铁继续腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气作水的杀菌消毒剂 | B. | 硅胶作袋装食品的干燥剂 | ||
| C. | 二氧化硫作纸浆的漂白剂 | D. | 肥皂水作蚊虫叮咬处的清洗剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
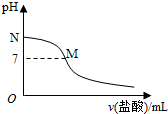
| A. | 该滴定过程应该选择酚酞作为指示剂 | |
| B. | M点对应的盐酸体积为20.0mL | |
| C. | M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-) | |
| D. | N点处的溶液中pH<12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
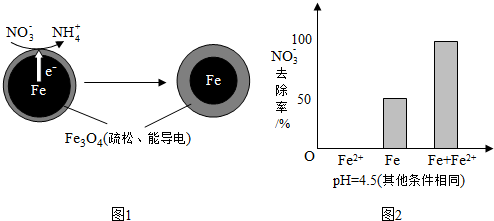
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 | 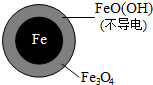 |  |
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 约10% | 约3% |
| 1小时pH | 接近中性 | 接近中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
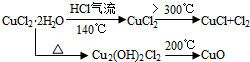
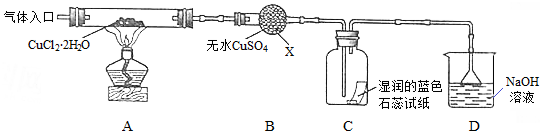
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化是物理变化 | |
| B. | 蛋白质的基本结构单元是氨基酸 | |
| C. | 在蛋白质溶液中加入CuSO4溶液,可使蛋白质的溶解度降低而析出 | |
| D. | 乙醛、葡萄糖、淀粉都能与新制的银氨溶液发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
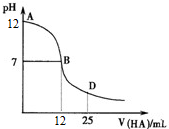
| A. | MOH在水中的电离方程式是MOH═M++OH- | |
| B. | 在B点表示酸碱恰好中和 | |
| C. | 随着盐酸的加入,溶液的导电能力逐渐增强(忽略体积变化) | |
| D. | 在D点时,存在c(OH-)>c(Na+)>c(Cl-)>c(M+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2具有氧化性,可用于漂白纸浆 | B. | NH4HCO3受热易分解,可用作氮肥 | ||
| C. | Fe2(SO4)3易溶于水,可用作净水剂 | D. | Al2O3熔点高,可用作耐高温材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com